Awaous lateristriga : caractérisation des paramètres de reproduction
3.3.Caractérisation de quelques paramètres de reproduction
3.3.1.Taille de première maturité sexuelle et Indice Gonado-somatique
La taille de première maturité sexuelle a été de 6 cm chez les femelles et de 6,1 cm chez les mâles.
La période de reproduction de A. lateristriga a été déterminée à partir des calculs de l’IGS sur des individus des deux sexes entre avril et mai (Tableau 9).
Chez les femelles, l’IGS moyen mensuel correspondant à la période de collecte décroit d’avril (7,79 %) à mai (4,83%) avant de reprendre une croissance en juin (5,75 %), tandis que chez le mâle, il décroit jusqu’en juin.
Les valeurs obtenues pour l’IGS du mâle sont plus faibles que chez la femelle pendant toute la période de collecte.
Tableau 9:Evolution de l’Indice Gonado-Somatique en fonction du temps
| IGS (%) | |||
| avril | mai | juin | |
| Femelles | 7,79 | 4,83 | 5,75 |
| Mâles | 4,14 | 2,53 | 1,45 |
3.3.2.Structure ovarienne
La figure 8 illustre la distribution des fréquences des diamètres des ovocytes dans l’ovaire d’une femelle au stade IV de maturité sexuelle (photo 1). On note des ovocytes de coloration blanchâtre, presque sphériques (photo 2) de diamètre supérieur à 0,1 mm prêts à être expulsés.
C’est ceux qui sont comptés pour établir la fécondité absolue. On note aussi des ovocytes de diamètre inférieur à 0,1 mm qui génèreront de nouveaux ovules. Une telle structure ovarienne bimodalesuggère une ponte unique dans l’année.
La majorité des ovocytes arrive à maturité au même moment avant la ponte. On ne retrouve plus qu’une petite quantité d’ovocytes non mûrs au moment de la ponte. Le diamètre moyen des ovules au moment de la ponte est de 0,28 ±0,11 mm.

Photo3: Aperçu de gonades au stade ovocytaire IV

Photo 4: Aperçu (à la loupe) de la morphologie des ovocytes de Awaous lateristriga.Grossissement (1,5x/10x)
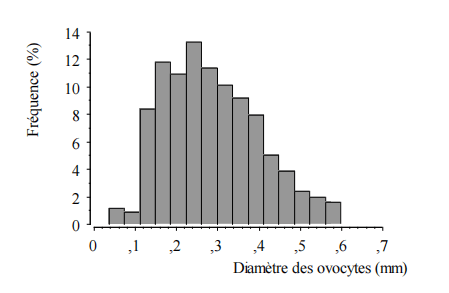
Figure 7: Distribution des fréquences de diamètre des ovocytes dans l’ovaire d’une femelleau stade IV de maturité sexuelle
3.3.3.Estimation de la fécondité
La fécondité absolue a été estimée à partir de 7 gonades toutes aux stades III et IV de maturité sexuelle. La taille moyenne des femelles utilisées pour cette estimation de la fécondité est de 7,37±1,32cm pour un poids moyen de 4,38 g±1,65 et un poids moyen des gonades de 0,42 g±0,37.
La fécondité absolue moyenne est de 24549 ovules ±33273 par poisson et la fécondité relative moyenne est de 7702 ±15790 ovules par gramme de poids corporel.
La fécondité absolue maximale observée est de 97307 ovules chez une femelle qui mesure 8,5 cm avec un poids total de 5,52 g et dont les gonades pèsent 0,80 g.
Partie 4 : Discussion
4.1Variation du régime alimentaire
Le profil général du régime alimentaire de A. lateristriga permet d’affirmer pour la période de l’étude que cette espèce est planctonophage à tendance phytoplantonophage. L’examen qualitatif de son régime alimentaire révèle que les espèces de phytoplancton font à elles seules 94,38% du régime alimentaire.
Ces résultats sont conformes à ceux de Christop et al.(1991) qui qualifie les gobiidae de planctonophages. Des variations du régime alimentaire se sont faites remarquées en fonction de la taille des individus.
Cet état de chose pourrait s’expliquer chez les individus de petites tailles par le fait qu’une forte alimentation est indispensable pour leur stade de développement et pour leur croissance (Declerck et al., 2002).
Les variations en fonction des saisons et du sexe peuvent être liées, entre autres aux phénomènes physiologiques de l’espèce que sont la reproduction et la migration (Pallaoro et al., 2003) .
Les valeurs nulles du coefficient de vacuité reflètent bien la disponibilité et la fréquence des aliments dans le milieu (Dia et Ghorbel, 2010).
Cet opportunisme a été mis en évidence par Barreiros et al., 2003 chez la sériole aux Açores (Seriola dumerili), où les auteurs ont noté un changement inter annuel au niveau des aliments préférentiels.
Par ailleurs, il semble que ce poisson présente une alimentation de type opportuniste. La présence de certains aliments dans les contenus stomacaux en tant qu’aliments préférentiels correspondrait à son abondance dans le milieu (Traoré et al., 2001).
En effet, l’importance numérique de Gyrosigma sp (Diatomée) dans le bol alimentaire de A. lateristriga se justifierait donc par son abondance dans le milieu d’étude.
Aussi faut il souligner que les poissons, d’une façon générale, sont opportunistes (Lauzanne, 1988) et consomment préférentiellement les proies les plus abondantes et disponibles localement (Psquaud et al., 2004). Bien qu’étant abondante dans le contenu digestif de A. lateristriga, Gyrosigma sp ne représente pas une espèce préférentiel du poisson.
4.2Relations poids-longueurs et Coefficient de condition (K)
L’étude des relations poids et longueur totale a permis d’apprécier le type de croissance chez A. lateristriga. En effet, les poissons étudiés, grandissent plus vite en longueur qu’en poids ce qui ne s’accorde pas avec les résultats de Lédéroun et al., (2016) pour des individus pris dans le même cours d’eau (fleuve Mono).
Les variations du coefficient de condition se justifieraient par l’état physiologique des poissons a été fortement influencées par les conditions environnementales, telles que les précipitations, l’alimentation (Papageorgiou, 1979) et par la productivité, et à la maturation sexuelle (El-Agami, 1988; Hadi, 2008; Shalloof et Salama, 2008).
4.3Taille de première maturité sexuelle etIndice Gonado Somatique
Les valeurs de taille de première maturité sexuelle indiqueraient que les mâles et les femelles atteignent la maturité sexuelle presqueà une même taille (6 cm).
La variation de l’IGS des femelles et des mâles de A. lateristriga dans le cour inférieur du fleuve Mono indique que l’espèce présente une période de ponte qui part d’avril à juin.
Ce résultat est conforme aux observations faites par Yamazaki (2011) qui a trouvé que Awaous melanocephalusa une période de reproduction qui s’étend d’avril à janvier.
La mise en parallèle de l’évolution de l’IGS avec la hauteur d’eau dans le milieu d’étude montre que la période de ponte coinciderait avec la grande saison des pluies qui va de la mi-mars à la mi- juillet (Gnélé, 2005).
Cela suppose que chez A. lateristriga les pluies sont favorables et stimulatrices de la ponte contrairement à la période de ponte de la plupart des poissons dont la maturation des gonades s’effectue à cette période.
La synchronisation de la période d’activité sexuelle avec la saison des pluies chez les poissons tropicaux a été démontrée chez beaucoup d’espèces (Lalèyè et al., 1995 ; Alkins-KO, 2000 ; Paugy et Levêque, 2004 ; Adité et al., 2006 ; Montchowui et al., 2006).
4.4Structure ovarienne et estimation de la fécondité
La distribution des fréquences de diamètres des ovules de A. lateristriga montre une distribution à un seul mode (ovules de petites tailles). Une telle structure ovarienne suggère une ponte unique dans l’année (Montchowui et al., 2006).
La majorité des ovocytes arrivent à maturité au même moment avant la ponte. On y trouve une petite quantité d’ovocytes non mûrs au moment de la ponte qui généreront de nouveaux ovules pour l’année suivante.
Les œufs de A. lateristriga sont petits (0,1 à 0,4mm de diamètre) et presque sphériques de même que ceux de A. melanocephalus (Yamazaki et al., 2011) pour un diamètre moyen de 0,4 mm.A. guamensis du fait de sa grande taille a une fécondité absolue moyenne plus élevée (689500 ; 217 mm) (Ha et Kinzie, 1996 ) que celle de A. lateristriga (97307 ovules ; 0,48 mm) et celle de A. melanocephalus(de (290000 ovules ; 127,8mm)dont les tailles sont inférieures à 150 mm (Yamazaki et al., 2011). Il apparaît que la fécondité dans le genre Awaous varie avec la taille du corps de la femelle.
Conclusion et suggestions
L’étude de la biologie de l’alimentation et de la reproduction de Awaous lateristriga (Duméril, 1861) a permis de disposer d’informations sur : le profil alimentaire, les préférences, le type de croissance, la structure de l’ovaire et la fécondité de l’espèce.
Au terme de cette étude, il en ressort que A. lateristriga a un régime alimentaire à tendance phytoplanctonophage beaucoup plus prononcé sur les cyanophytes et les diatomées.
Des variations du régime chez les individus se sont faites notées tant bien pour les périodes d’échantillonnage, pour la taille que pour le sexe. A. lateristriga est un poisson à ovogenèse synchrone et à fécondité relativement élevée.
C’est une espèce de petite taille qui de par son caractère opportuniste s’adapte à toutes les conditions d’alimentation du milieu. Elle pourrait donc être exploitée comme espèce piscicole.
De plus, cette étude de par ses résultats constitue une base de données préliminaire et technique d’alimentation et de reproduction afin de poursuivre le processus de sa domestication. Toutefois, à long terme, nous suggérons :
- D’étendre l’étude sur un cycle annuel afin de mieux distinguer les aliments constitutifs du régime alimentaire sur différentes périodes de l’année;
- D’étudier le rythme alimentaire de l’espèce ce qui permettra de définir les périodes d’intenses activités de l’espèce ;
- Faire l’échantillonnage sur différentes périodes de l’année afin de déterminer la taille de la première maturité sexuelle et d’évaluer dans le temps le rapport gonado- somatique afin de déterminer la période exacte de reproduction de l’espèce.
