Les avortements spontanés à répétition (ASR): étude statistique et étude cytogénétique
Partie pratique: Patients et méthodes
Notre travail de recherche est répartie en deux volets complémentaires : une étude statistique suivie d’une étude cytogénétique. 7 couples enrôlés dans cette étude sont recrutés au niveau du service de gynécologie du CHU Benbadis ainsi que de la maternité Sidi Mabrouk – Constantine.
Le seul critère d’inclusion retenu est le fait que ces couples ont vécus ≥ 2 avortements spontanés répétés inexpliqués. Nous avons exclu de cette prospection les couples qui ont refusé de participer à cette étude.
1- Étude statistique
Ce volet de notre étude vise à prospecter sur une cohorte de couples ayant vécus plusieurs fausses couches spontanées à répétition, par la réalisation d’un questionnaire (annexe I), les étiologies possibles à ce dysfonctionnement de la santé reproductive.
Plusieurs types de données sont recueillis : les paramètres anthropométriques de la femme, son état de santé, ses habitudes alimentaires, l’aspect de l’utérus à l’échographie. Les valeurs du bilan hormonal sont relevés.
La recherche du syndrome métabolique est faite. Des précisions concernant le recours à une procréation médicalement assistée sont demandées (nombre de tentatives, type de PMA, taux de réussite).
Des informations sur la santé reproductive du conjoint sont également demandées.
Enfin, des renseignements sur la santé reproductive de la fratrie sont sollicités dans la perspective d’une possible étiologie génétique familiale héréditaire. Les données ainsi recueillies sont traitées par Excel.
2- Étude cytogénétique
Ce volet de notre étude vise à l’application des techniques de cytogénétique pour la réalisation du caryotype sur des prélèvements sanguins issus de couples avec antécédents plusieurs FCS.
L’analyse cytogénétique s’est faite au niveau de l’unité de cytogénétique du CRBt – Constantine.
Les prélèvements sanguins sont recueillis dans des conditions stériles par ponction veineuse, dans des tubes de 4 ml contenant l’héparine de lithium ou l’héparine de sodium comme anticoagulants.
Ces prélèvements sont acheminés dans l’immédiat au CRBt pour la mise en culture cellulaire.
2-1- Matériel et réactifs
2-1-1- Matériel
– Tubes coniques de 15 ml (aliquotes du milieu de culture),
– Lames de microscope 26×76 mm (labbox®),
– Boites de rangement des lames,
– Micropipettes (20-200 μl),
– Pipettes de transfert en plastique,
– Hotte à flux laminaire (ALS- STERIL- HELIOS®),
– Hotte chimique (Shinsaeng®-model : SFH-2012 (UP)),
– Centrifugeuse à grande vitesse (SIGMA® 2-16 KL),
– Vortex (IKA®), (VELP®, WIZARD Advanced IR Vortex Mixer),
– Station cytogénétique motorisé (Leica® DM6000b) reliée à un ordinateur disposant d’un système de traitement d’image (logiciel Cytovision®),
– Étuve (Memmert®),
– Réfrigérateur à 4ºC,
– Congélateur à -20ºC,
– Bain marie (Memmert®),
– Becher en verre (20 ml, 25 ml, 100 ml, 600 ml et 1000 ml),
– Becher en plastique (50 ml, 100 ml et 400 ml),
– Pince,
– Cuve à coloration (Hellendahl®),
– Papier absorbant,
– Éprouvettes graduées en verre (250 ml, 500 ml),
– Bac en verre,
– Portoir pour tube,
– Pipette graduée 0,5 ml,
– Présentoir de lames,
– Gant nitrile non stérile (non poudré),
– Embouts à Pipette (ISOLAB® 200μl).
2-1-2- Réactifs
– PBMax : préparé 8 ml, conservé à -20 °C
– Thymidine (100 μl) : 0,6 g dans 100 ml de PBS (Phosphate Buffered Saline)
– PBS : 1 comprimé de PBS dans 200 ml d’eau bidistillée (Sigma®),
– Eau distillée,
– Eau minérale,
– Eau bidistillée,
– Acide acétique 100%,
– Éthanol pure 99-100°.
– Giemsa liquide Fluka®.
– Huile d’immersion,
– Sérum de Veau Fœtal (SVF) (1,5 ml),
– RPMI 1640 Medium avec L-glutamine et sodium bicarbonate (6,5 ml),
– Colchicine (60 μl) : 0,1 g dans 100 ml d’eau distillée,
– – KCl : 5,6 g/l,
– Sodium phosphate monobasique di-hydraté (NaH2PO4+2H2O) : 78 g de poudre de phosphate
+ 500 ml d’eau distillée
– Carnoy : 3V Éthanol +1V d’Acide acétique.
– Tampon de Gürr,
– Giemsa : 10 ml solution de Gürr + 5 ml de Giemsa + eau minérale.
2-2- Méthodologie
Tous nos prélèvements ont été réalisés par des infirmiers par ponction veineuse dans des conditions stériles et en utilisant des tubes héparinés au lithium ou au sodium.
2-2-2- Mise en culture
– La mise en culture a été être réalisée avec du sang frais le jour même du prélèvement.
– Étiqueter les tubes du milieu de culture avec le numéro d’organisation.
– Travailler sous hotte à flux laminaire horizontale, ouvrir les tubes et éviter de passer les mains au-dessus des tubes.
– Mettre 10 gouttes de sang dans le milieu de culture PBMax.
– Fermer les tubes et les incuber horizontalement (légèrement inclinés) dans une étuve à 37°C pour une période de 72 heures.
– Ajouter 100 µl de Thymidine après 48h de mise en culture et les remettre en culture.
2-2-4- Lavage
– Retirer les tubes de l’étuve,
– Procéder à la centrifugation des tubes à 1500 tours par minute (tpm) durant 5 minutes 30,
– Verser le surnageant, ajouter environs 1 ml de PBS (le PBS aide à enlever la thymidine),
– Vortexer pour bien mélanger,
– Mettre 10 ml de PBS (jusqu’à l’étiquette) et bien mélanger,
– Centrifuger une deuxième fois et procéder à un deuxième lavage « aspiration du surnageant, dilution au PBS, mélanger au vortex, rajouter du PBS et remettre à la centrifugeuse ».
– Après centrifugation rajouter 1,5 ml de RPMI et vortexer,
– Compléter avec 5 ml de RPMI et 1,5 ml de SVF.
2-2-6- Blocage en métaphase
– Après incubation de 5h à 5h30, sous haute à flux laminaire ajouter 60 µl de colchicine pure à l’aide d’une micropipette (20-200 μl) dans chaque tube, homogénéiser et remettre à l’étuve en position horizontale pendant 30 minutes.
2-2-7- Choc hypotonique et préfixation
– Centrifuger les tubes de culture à 1500 tpm pendant 5 minutes 30. Sous hotte chimique, verser le surnageant et ajouter 1 à 2 ml de KCl à la concentration de 5,6 g/l préchauffé à 37°C.
– Vortexer et compléter avec 10 ml de KCl,
– Homogénéiser par retournements puis incuber en position horizontale pendant 20 minutes.
2-2-8- Préfixation
– Procéder à la préparation du carnoy en mélangeant 3V d’éthanol avec 1V d’acide acétique,
– Ajouter 0,5 ml à 1 ml de carnoy et homogénéiser par retournements,
– Centrifuger les tubes de culture à 1500 tpm pendant 5 minutes 30, puis, sous la hotte, verser le surnageant.
2-2-9- Fixation
– Ajouter 1 à 2 ml de carnoy, vortexer et compléter avec du carnoy,
– Homogénéiser par retournements et fixer à température ambiante pendant 20 minutes,
– Centrifuger les tubes de culture à 1500 tpm pendant 5 minutes 30,
– Sous hotte chimique, verser le surnageant et refaire une de deuxième fixation : ajouter le carnoy, vortex, compléter jusqu’à 10 ml et on met au réfrigérateur à 4°C.
2-2-10- Étalement
– Préchauffer jusqu’à 86°C. Placer les lames dégraissées et les préchauffer en l’exposant à l’humidité du bain marie. Laisser tomber deux gouttes de culot à une certaine distance (~20 cm) de chaque lame, rincer au carnoy,
– Bien sécher les lames sur le bord du bain marie.
NB : Il faut savoir que les conditions atmosphériques (température, humidité, pression atmosphérique) influent sur la qualité des étalements.
2-2-11- Coloration
* Coloration sans dénaturation
– Placer directement les lames séchées dans le Giemsa pendant 5 minutes,
– Sortir les lames et les rincer avec l’eau du robinet.
* Coloration avec dénaturation et (RHG)
– Réhydrater les lames dans de l’eau distillée durant 5 min.
– Plonger les lames dans la solution phosphate (NaH2PO4+2H2O) à 86°C pendant 14 minutes,
– Plonger les lames dans le Giemsa durant 5 minutes,
– Rincer les lames à l’eau du robinet.
2-2-12- Observation des lames après coloration
– Observer les lames sous microscope optique et traiter les captures avec le logiciel installé.
Après avoir choisi les lames à colorer, elles sont ensuite observées et étudiées par la station cytogénétique motorisée relié à un ordinateur traitant les images par le logiciel : Cytovision®.
On observe premièrement avec l’objectif (x10) puis, lorsqu’on repère une bonne mitose, on met une goutte d’huile d’immersion et on passe à l’objectif (x63) et après à l’objectif (x100).
2-2-13- L’interprétation des résultats
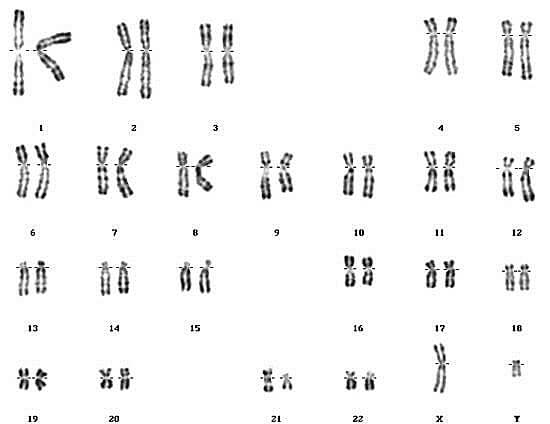
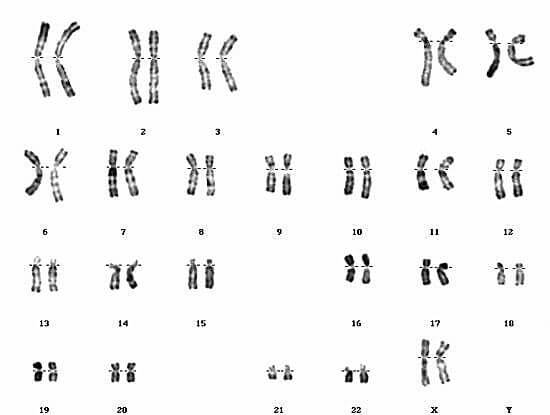
– La lecture des résultats et la prononciation sur la présence d’une éventuelle anomalie se fait par comparaison avec un caryotype de référence normal (figures 07 et 08).