Résultats et discussion : la dégradation du milieu aquatique
Chapitre 5 : résultats et discussion
5.1- La température
La température est un facteur physique fondamental dans les milieux aquatiques, c’est l’un des principaux paramètres explicatifs de comportement biologique de l’eau. En effet, elle influence l’activité des êtres vivants (les bactéries, les micro-algues, ….etc.).
L’évolution temporelle de la température au niveau de la serre ʺ le milieu artificiel ʺ présente des fluctuations en fonction du temps dont les valeurs varient entre 19.83 et 27.7 °C.
Par contre, dans le milieu naturel ʺ extérieur de la serre ʺ, les températures sont moins élevées ; les valeurs varient entre 13.5 et 18.4 °C (Tableau 4 ; figure 22). En fait, les essais sous serre milieux montrent une évolution de la qualité de l’eau ce qui explique une dégradation rapide de la matière organique présente dans le milieu.
Tableau 4 – Température journalière dans la serre et à l’extérieur pendant 25 jours d’expérimentation.
| Durée Expérimental (jours) | T°C moyenne
(la serre) |
T°C moyenne
(milieu extérieur) |
| 1 | 22.1 | 15.6 |
| 2 | 19.83 | 13.5 |
| 3 | – | 11.8 |
| 4 | – | 12.1 |
| 5 | 27.93 | 13.4 |
| 6 | 22.03 | 14.7 |
| 7 | 22.6 | 17 |
| 8 | 21.4 | 17.6 |
| 9 | 22.93 | 16.8 |
| 10 | – | 14.1 |
| 11 | – | 12.3 |
| 12 | 22.86 | 15.1 |
| 13 | 23.34 | 15.5 |
| 14 | 22.03 | 17.2 |
| 15 | 24.53 | 17.6 |
| 16 | – | 15.3 |
| 17 | – | 17.8 |
| 18 | – | 17.7 |
| 19 | 24.83 | 17.5 |
| 20 | 27.7 | 14 |
| 21 | 25.8 | 14.9 |
| 22 | 27.63 | 18.4 |
| 23 | 22.7 | 17.6 |
| 24 | – | 16.3 |
| 25 | – | 16.1 |
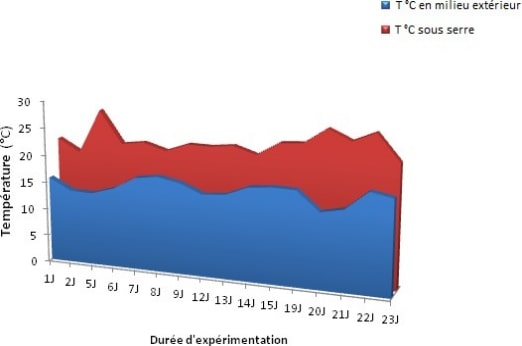
Figure 22 – le changement de la température de l’air au niveau de la serre et le milieu naturel.
5.2- La couleur
La coloration d’une eau peut être soit d’origine naturelle (éléments métalliques, matières humiques, microorganismes liés à un moment de dégradation …. etc.), soit associée à la pollution (composés organiques colorés). Elle est donc très souvent synonyme de la présence des composés dissous (Thomas, 1995).
Durant toute l’expérimentation dans la serre et en milieu extérieur, on observe des changements de couleur dans les différents essais, résultant ne seulement de la dégradation de la MO provenant, soit du végétal soit de l’eau usée mais aussi d’une apparition de micro-algues dans le milieu (Tableau 5 ; figures 23 et 24).
Dans le cristallisoir contenant de l’eau en présence du végétal, la couleur de l’eau vire au marron foncé. Ceci peut être expliqué par la dégradation de la MO en acide fulvique, acide humique et en substances humines qui sont des polymères organiques issus d’une dépolymérisation de la matière végétale, résultant de la transformation physique, chimique et microbiologique des résidus végétaux (Tahiri et al., 2014) et d’accumulation oxydative de plusieurs composés : acides aminés, peptides et des polysaccharides, riches en carbone.
Par contre dans le cristallisoir contenant de l’eau d’égout, l’eau présente une teinte verdâtre qui est due à la prolifération d’algues microscopique, signe d’une dégradation de l’eau.
Tableau 5 – Variation de la couleur de l’eau des échantillons dans le milieu artificiel et le milieu naturel pendant les 25 jours. (E = eau ; EU = eau usée; V = végétal ; O = à l’obscurité ; L = à exposé de la lumière); E (75%) + EU (25%) : 3 litre E + 1 litre EU ;E (81.25%) + EU (18.25%) : 3.25 litre E + 0.75 litre EU ;
E (87.5%) + EU (12.5%) = 3.5 litre E + 0.5 litre EU ;E (93.75%) + EU (6.25%) = 3.75 litre E + 0.25 litre EU.
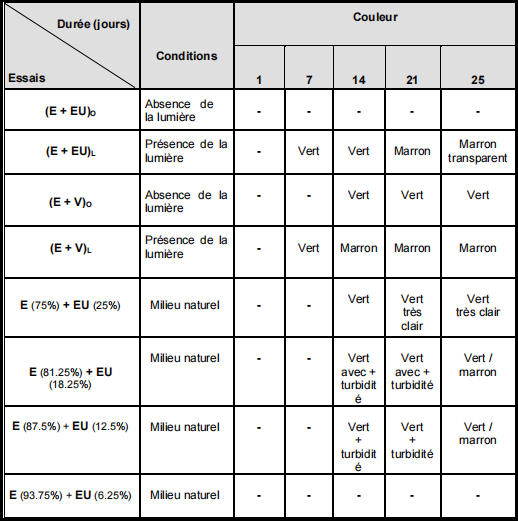

Figure 23 – Changement de couleur de l‘eau après la dégradation de végétal et la prolifération des algues

Figure 24 – Evolution de la couleur de l’eau en fonction des différentes concentrations des eaux usées en milieu naturel (6.25%, 12.5%, 18.25%, 25%).
5.3- La turbidité
La turbidité est le caractère trouble de l’eau. Elle est causée par les matières en suspension telles que les particules organiques (MOP et COD), le plancton et les autres organismes microscopiques. Elle est également due à la présence des matières colloïdales d’origine organique ou minérale.
Une turbidité trop élevée empêche la pénétration de la lumière dans la colonne d’eau et peut ainsi diminuer la croissance des algues et des plantes aquatiques (Vilagines, 2003).
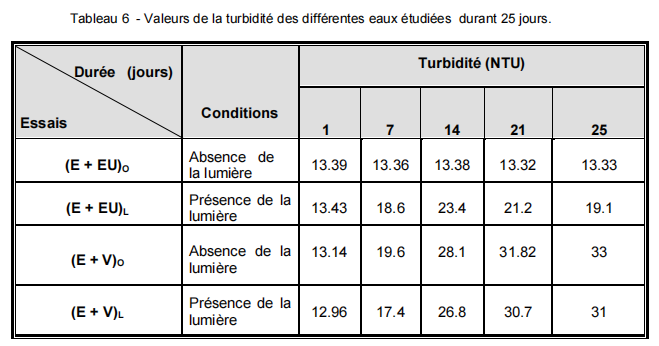
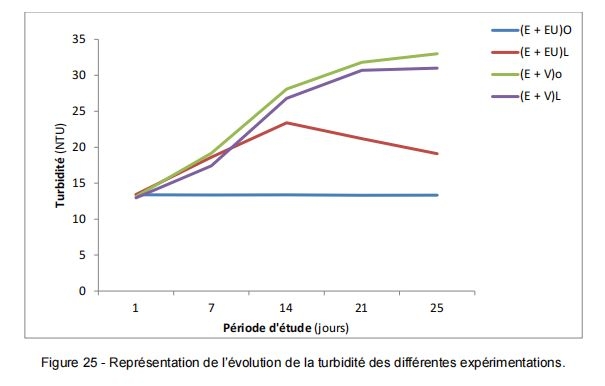
La dégradation du végétal, soit avec la présence de la lumière ou en obscurité, indique des valeurs très élevées de la turbidité comprise entre 31 et 33 NTU en Tf par apport aux valeurs obtenues par la dégradation de la MO dans les eaux usées à l’obscurité et en présence de lumière correspondant respectivement à des valeurs de 13.33 et 19.1 NTU. Sachant que les premières mesures de la turbidité de l’eau étudiées enregistrent des valeurs faibles variant entre 12.96 et 13.43 NTU (tableau 6 et figure 25).
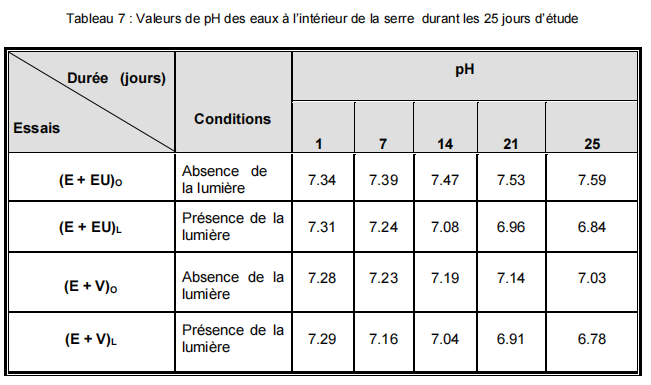
5.4- Le pH
Le pH montre l’équilibre entre les acides et les bases d’un plan d’eau et une mesure de la concentration des ions hydrogène en solution. En fait, le potentiel d’hydrogène dépend de plusieurs facteurs tels que l’oxygène dissous, le gaz carbonique et le taux de la MO.
Ainsi, une chute de pH pourra conduire une augmentation de la teneur en CO2 et une diminution du taux d’O2 (Delamare de Boutteville, 1960).
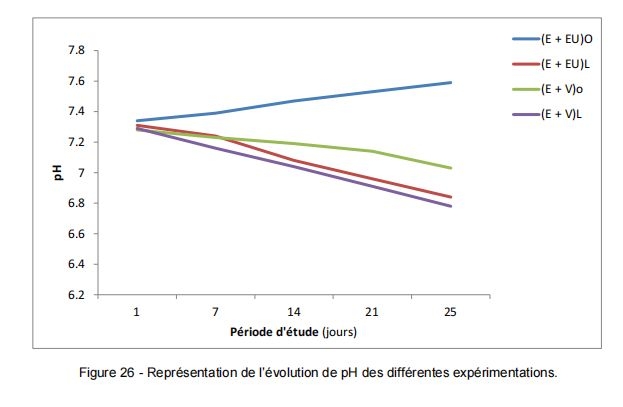
Dans notre étude, on constate que pendant 25 jours, le pH apparait inégalement dans les différentes eaux étudiées. Alors, on enregistre une chute de pH dans les eaux : Eau + eau usée en présence de lumière), Eau + végétale en obscurité et Eau + végétale en présence de lumière, allant de 7.31 (en T0) à 6.78 (en Tf) (Tableau 7 ; figure 26).
L’apparition de cette acidité dans l’eau est due à des composés azotés (azote ammoniacal…) issus certainement à l’activité bactérienne dans le milieu.
5.5- L’oxygène dissous
L’oxygène dissous dans l’eau est un élément fondamental qui intervient dans la majorité des processus biologique. L’oxygène participe également aux dégradations de MO par phénomènes biochimiques et chimiques.
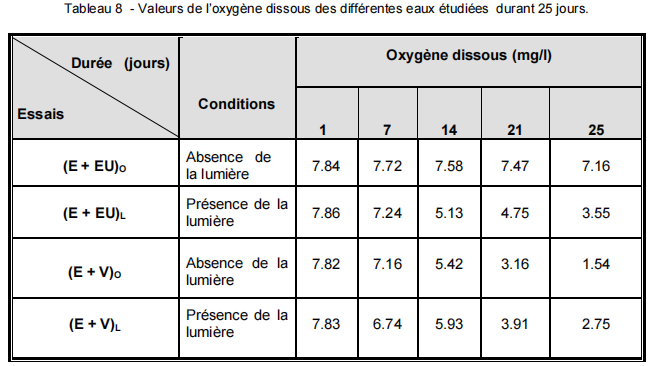
Dans les eaux contenant le végétal, les teneurs en oxygène dissous sont aux alentours de 7.82 mg/l en To. Le taux d’oxygène diminue considérablement en Tf ; les valeurs enregistrées restent entre 1.54 et 2.75 mg/l. Cette diminution du taux d’oxygène découle du fait de l’oxydation de la matière organique.
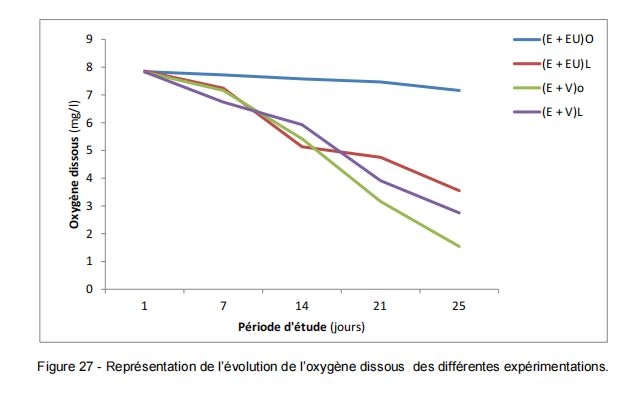
Les eaux contenant 25% d’eaux usées présentent en Tf, des valeurs comprises entre 7.16 et 3.55 mg/l d’oxygène correspondant respectivement à l’absence et à la présence de la lumière (Tableau 8 ; figure 27).
Cette chute légère d’oxygène explique que plus la quantité de la matière organique est réduite plus la demande chimique de l’oxygène (DCO) est faible. De ce fait, l’oxygène présent en To diminue très légèrement.
Tableau 8 – Valeurs de l’oxygène dissous des différentes eaux étudiées durant 25 jours.
5.6- Les substances nutritives
La présence des éléments nutritifs (l’azote ammoniacale, le nitrate, le nitrite et le phosphate) est un indicateur très important pour l’évaluation de la qualité des eaux et la dégradation de la matière organique.
En effet, la concentration de ces éléments augmente en provoquant l’apparition et le développement des micro-algues et des bactéries qui sont généralement responsables de l’eutrophisation des milieux aquatiques.
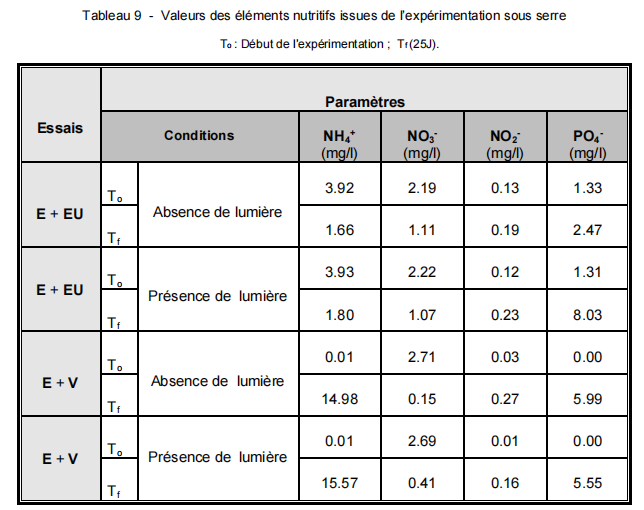
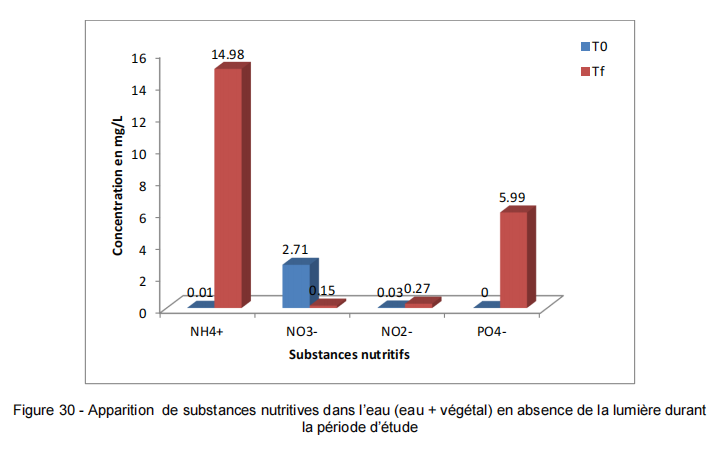
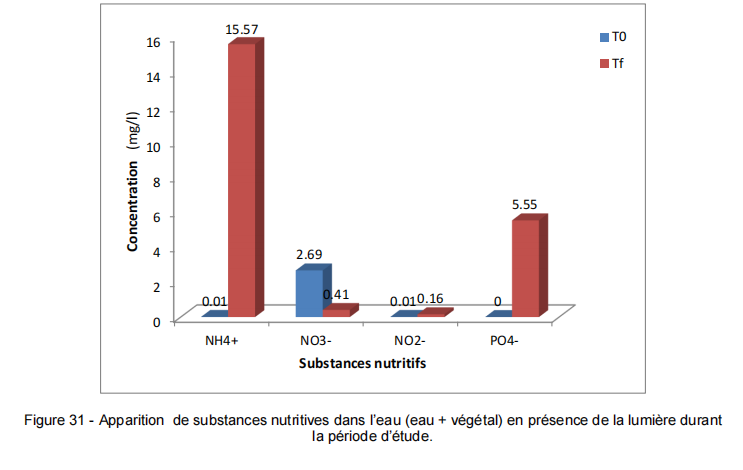
La dégradation de la MO naturel (végétal) soit en présence de la lumières ou à l’obscurité présente une augmentation élevée de la concentration de l’azote ammoniacal (NH +) dont les valeurs se situent entre 14.98 et 15.57 mg/l. Quant au phosphate (PO -), les concentrations observées varient entre 5.55 et 5.99 mg/l.
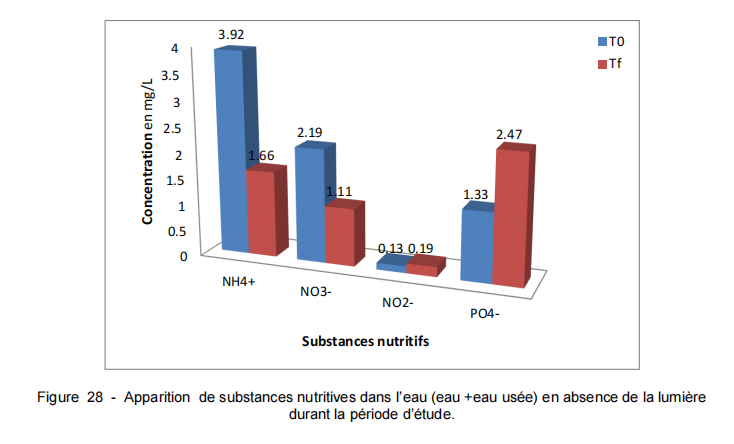
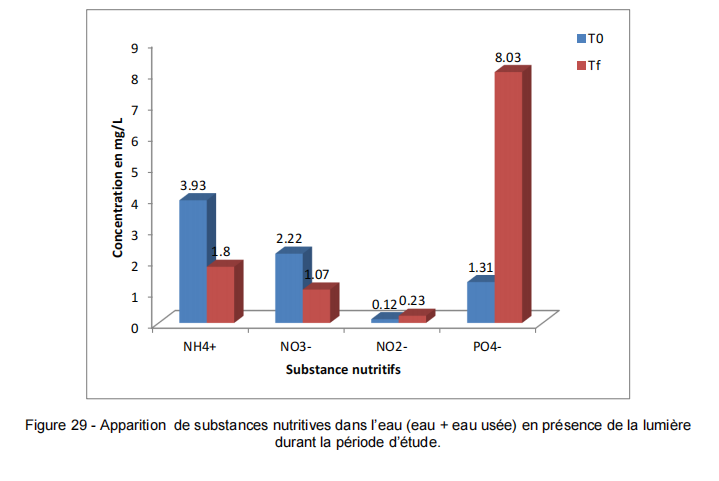
Les eaux contenant 25% d’eau usée en présence de la lumières ou à l’obscurité, enregistrent une diminution de la concentration de l’azote ammoniacale et le Nitrate et une légère augmentation de Nitrites. Mais ils donnent une augmentation de la concentration de phosphate 8.03 mg/l (la lumière) et 2.47 mg/l (obscurité).
Tableau 9 – Valeurs des éléments nutritifs issues de l’expérimentation sous serre
To : Début de l’expérimentation ; Tf (25J).
5.7- La flore totale
La Flore aérobie mésophile totale, également appelée Flore totale, est l’ensemble des micro- organismes, bactéries, levures et moisissures pouvant se développer dans des conditions moyennes de pH, salinité, humidité, en présence d’oxygène et pour des températures de croissance effective de 10 à 45°C.
Cette flore est composée de microorganismes banaux et de germes pathogènes. Ces derniers sont d’origine fécale dont le dénombrement est facilité par l’utilisation de germe indicateur de pollution.
Les analyses bactériologiques des eaux à la fin de l’expérimentation donnent un nombre élevé des colonnes de la flore total estimé plus ou moins 1000 UFC/ml dans 3 types d’eau « Eau + eau usée (à l’exposition de la lumière), et les deux types d’eau contiennent le végétal comme MO (à l’exposition de la lumière et à l’obscurité) », par contre dans le dernier type d’eau (Eau + eau usée à l’obscurité) on estime entre 550 et 600 UFC/ml.
5.8- Les coliformes
Les coliformes totaux sont des entérobactéries qui incluent des espèces dans l’environnement en général (sols, végétation et l’eau). Ce groupe bactérien est utilisé comme indicateur de la qualité microbienne de l’eau parce qu’il contient notamment des bactéries d’origine fécale.
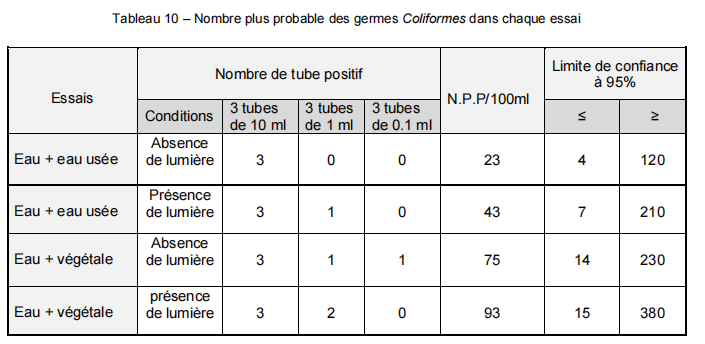
Les analyses bactériologiques des eaux étudiées au niveau de milieu artificiel donnent des différentes valeurs de NPP dans 100 ml pour chaque type d’eau (Tableau 10).
5.9- Les streptocoques fécaux
Ces bactéries sont des cellules procaryotes ovoïdes, sphériques ou lancéolées, non mobiles et non sporulées, prenant la coloration de Gram (cocci à Gram positif). La recherche des streptocoques fécaux associés à celle des coliformes constitue un bon indice de contamination fécale (Rodier, 2005).
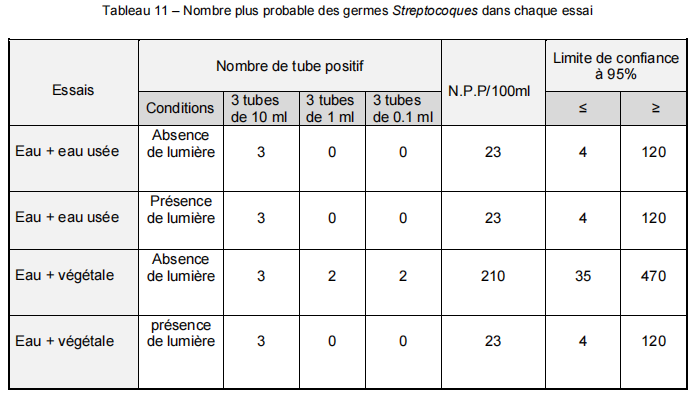
La dégradation de la matière organique naturelle, exemple le végétal » en absence total de la lumière donne un nombre élevé de germes Streptocoques dans l’eau par apport aux autres essais de l’eau analysées qui donnent le même Nombre plus probable des streptocoques dans chaque 100 ml (Tableau 11).
Tableau 11 – Nombre plus probable des germes Streptocoques dans chaque essai
5.10- Identification des micro-algues
Les algues microscopiques et les cyanobactéries désignent une série d’espèces variées de végétaux unicellulaires ou pluricellulaires, de taille généralement comprise entre 0,5 μm et 1 mm. Elles colonisent dans les milieux marins, les eaux douces et ainsi les eaux contaminées.
En effet, leur développement excessif relatif avec des conditions de la température, la lumière, la concentration de la matière organique et les éléments nutritifs (Mata et al, 2010).
L’observation microscopique permet de nous donner une idée sur les micro-algues qui caractérisent les eaux contaminées, alors il y a une présence des espaces de deux classes des micro-algues sont les bacillariophycées (qui contiennent 3 genres) et les chlorophycées (qui contiennent un seul genre) par une abondance différente (Figures 32 à 36 ; Tableau 12).
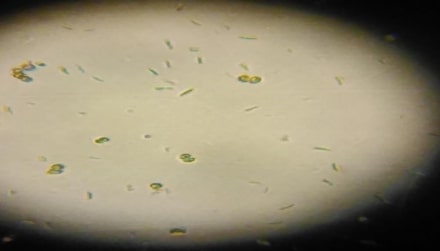
Figure 32 – observation microscopique des micro-algues (endroit 1) GX10 Genres : Asterococcus, Diatoma.

Figure 33 : observation microscopique des micro-algues (endroit 2) GX10 Genres : Asterococcus, Diatoma
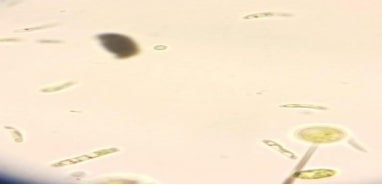
Figure 34 : observation microscopique des micro-algues GX40 Genres : Eutonia, Diatoma, Cocconies, Asterococcus.
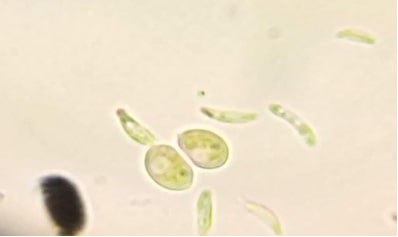
Figure 35 – observation microscopique des micro-algues (A) GX100 Genres : Eutonia, Diatoma, Asterococcus.
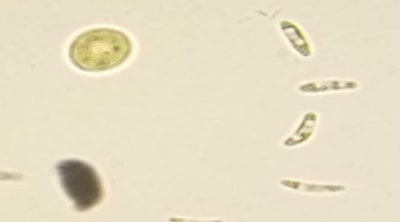
Figure 36 – observation microscopique des micro-algues (B) GX100 Genres : Eutonia, Diatoma, Asterococcus.
Tableau 12 – Biodiversité des micro-algues dans les eaux contaminées
| Microalgues | Genre | Abondance |
| Bacillariophycées | Diatoma | ++++ |
| Eunotia | ++ | |
| Cocconies | + | |
| Chlorophycées | Asterococus | +++ |
Discussion
La qualité de l’eau contaminée par une pollution organique quelle que soit à partir des matières organiques anthropiques ou naturelles décrite par un ensemble de variables physico- chimiques, biologique et biotique, et chaque paramètre relatif l’un avec les autres.
La température et la lumière et la quantité des polluants organiques sont les principaux paramètres qui augmentent les effets de la dégradation de la matière organique dans l’eau. En effet, ils favorisent la multiplication des bactéries et des micro-algues « prolifération » et accélèrent l’eutrophisation des eaux.
Suite aux résultats obtenus, une température journalière de 23°C avec la présence de a lumière peuvent provoque la prolifération des micro-algues à partir des eaux contenants 25 % d’eau usée entre 7 et 10 jours.
Les autres résultats obtenus donnent une Idée sur les effets de chaque type de la matière organique :
La dégradation de la matière organique naturelle par les microorganismes à une température entre
20 à 30°C en présence de la lumière ou en obscurité enregistre une augmentation de la concentration de l’azote ammoniacal et du phosphate. Il est à signaler également une augmentation de la turbidité et une chute du taux d’oxygène dissous et du pH. On assiste aussi à une multiplication excessive des bactéries.
La contamination des eaux par les eaux usées (Matière organique anthropique) enregistre une multiplication excessive des micro-algues qui sont généralement des diatomées, la présence de ces derniers est un indicateur de pollution.
Cette apparition des micro-algues provoque une diminution de l’oxygène dissous et du pH avec une augmentation de la turbidité. On enregistre aussi une multiplication des bactéries telles que la flore mésophile totale, les coliformes et les streptocoques fécaux.
Conclusion générale
Parmi les problèmes et les perturbations qui touchent les écosystèmes aquatiques c’est l’eutrophisation. C’est un problème majeur de la dégradation de l’environnement actuel, qui prend de plus en plus d’ampleur. Une forte eutrophisation a pour conséquence une réduction notoire du nombre d’espèces aquatiques végétales et animales.
L’étude des caractérisations physico-chimiques, bactériologiques et biologiques des eaux étudiées révèle des concentrations élevées de certains éléments chimiques (NH + et PO -) issus de la dégradation de MO végétale. En présence de la lumière ou en obscurité, la teneur en nitrate diminue par contre les nitrites augmentent légèrement
Dans le cas d’une contamination par les eaux d’égouts, la concentration de phosphore augmenté considérablement en présence de la lumière avec une dégradation des composées azotés. Ce qui caractérisé des eaux fortement minéralisées quelle que soit le type de contamination (anthropique ou naturelle).
La dégradation des matières organiques et la contamination par les égouts favorisent la multiplication des bactéries « la flore total, les coliformes et les streptocoques fécaux ». Cette apparition de germes entraine une diminution de l’oxygène dissous, qui est un indicateur d’un milieu eutrophie.
Les eaux contaminées par les eaux usées sont riches en éléments nutritifs, ce qui favorise la prolifération des micro-algues tels que les Chlorophycées et les Bacillariophycées « Diatomophycées » qui représente le genre dominant de la population algale.
A l’issu de cette prolifération, la turbidité s’élève de plus en plus dans le milieu. Par contre, on enregistre une teneur en oxygène faible, signes de l’eutrophisation.

