1. Chapitre I : Etat de l’art
1.1. Intérêt d’étudier les milieux aquatiques peu profonds
Les écosystèmes peu profonds désignent le type de systèmes d’eau douce largement affectés par les êtres humains pour des besoins sociaux, écologiques, et économiques.
Une de leur caractéristiques principales est la présence de plantes submergées qui sert de refuge pour de nombreux consommateurs aquatiques (Moss et al., 2011).
Au-delà du grand nombre de services écosystémiques (alimentation, reproduction, nurserie pour de nombreuses espèces) qu’ils rendent, ces milieux constituent des modèles pour le suivi des pressions climatique et agricole.
Le fait qu’ils soient étroitement liés aux habitats de subsurface les exposent et les rend vulnérables à l’accumulation de sédiments (Piggott et al., 2015) et de contaminants organiques et chimiques (Jeppesen et al., 2015).
Depuis une quarantaine d’années, les études écologiques sur les milieux peu profonds se sont intensifiées en réponse aux problèmes croissants posés par l’eutrophisation et par le changement climatique (Phillips et al., 2016).
1.2. Sensibilité des milieux aquatiques peu profonds et de leurs ressources aux forçages climatique et anthropique
Le changement climatique est une réalité de la vie sur terre tout comme l’évolution et l’extinction des espèces. Il se produit généralement sur des échelles de temps allant du siècle à des millions d’années.
Cependant, du fait de l’influence anthropique, le changement climatique qui touche actuellement notre planète survient beaucoup plus vite.
Il peut devenir très dangereux pour les écosystèmes aquatiques. C’est le cas par exemple du réchauffement climatique, principale variable du changement climatique (De Laurentiis et al., 2014).
Il s’agit d’une contrainte d’ordre globale qui pose aujourd’hui de sérieux problèmes en écologie, en particulier dans la structure et le fonctionnement de l’écosystème. Ce constat est particulièrement vrai pour les pays dont le développement dépend essentiellement des secteurs vulnérables au changement climatique.
Tel est le cas de l’agriculture dont l’intensification fait parfois recours à des pratiques agricoles qui pour la plupart du temps ne font pas bon ménage avec les principes de base de l’écologie.
Ces pratiques dites « mauvaises » engendrent des phénomènes néfastes tant sur l’environnement terrestre qu’aquatique (Evans et al., 2019).
En effet, dans un milieu aquatique qui fonctionne bien, la végétation immergée fournit une structure d’habitat aux consommateurs secondaires (poissons par exemple), de sorte que les consommateurs primaires (zooplancton et macroinvertébrés) maintiennent un contrôle descendant sur la croissance des algues.
Cependant, un milieu aquatique qui dysfonctionne (Figure 2) est très peu oxygéné et se caractérise notamment par (1) un nombre limité de poissons, (2) une prédominance de cyanobactéries, (3) et une abondance de la végétation flottante (Nuttens et al., 2016), moins efficace comme refuge pour les consommateurs (Meerhoff et al., 2007) lesquels ne contrôlent plus efficacement la croissance algale (Phillips et al., 2016).
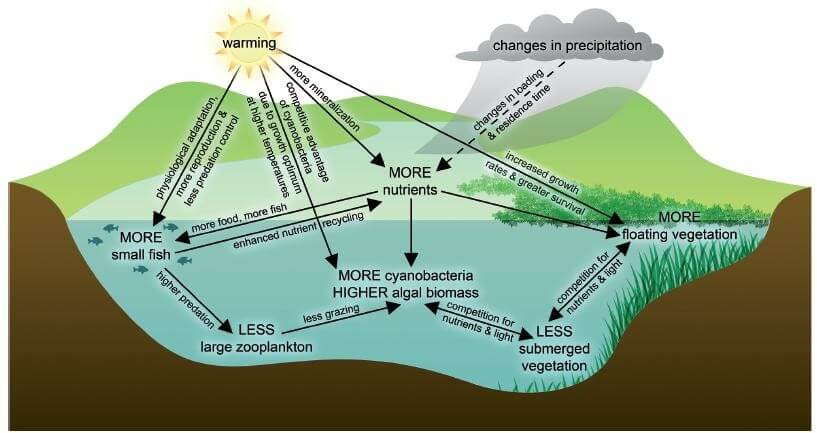
Figure 2: Représentation d’un milieu aquatique peu profond subissant des perturbations globales et locales. Source : Moss et al. (2011)
Les causes de contamination des milieux aquatiques par les substances toxiques utilisées en agriculture sont multiples (Figure 3).
Elles se caractérisent notamment par la dérive des produits lors de leur épandage, leur volatilisation, leur entrainement par la pluie (ruissellement et infiltration) et par le phénomène d’érosion (Scholtz and Bidleman, 2007).
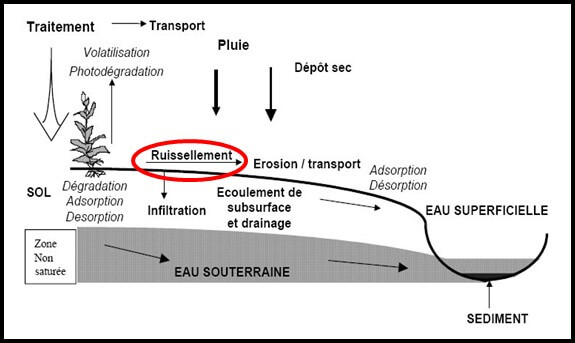
Figure 3: Causes de pollution des milieux aquatiques peu profonds liées aux pratiques agricoles
Source : https://www.vienne-nature.fr/pesticides/
Au nombre des raisons sus-citées, ce sont les eaux de ruissellement provenant des terres agricoles qui sont les principales sources de pollution des systèmes aquatiques peu profonds (Mas-Pla and Menció, 2019).
Elles sont essentiellement chargées en éléments nutritifs (nitrate, phosphate) et en substances toxiques (contaminants métalliques et produits phytosanitaires) utilisés de nos jours pour maintenir, optimiser et rentabiliser la production agricole.
Une fois que ces additifs ont atteint les milieux aquatiques peu profonds, ils donnent lieu à des contraintes locales (effets neutres, additifs, antagonistes ou synergiques) qui peuvent s’amplifier ou être inhibées lorsqu’elles interagissent avec le réchauffement climatique (Figure 4), défavorisant ainsi les ressources aquatiques qui s’y retrouvent (Knillmann and Liess, 2019).
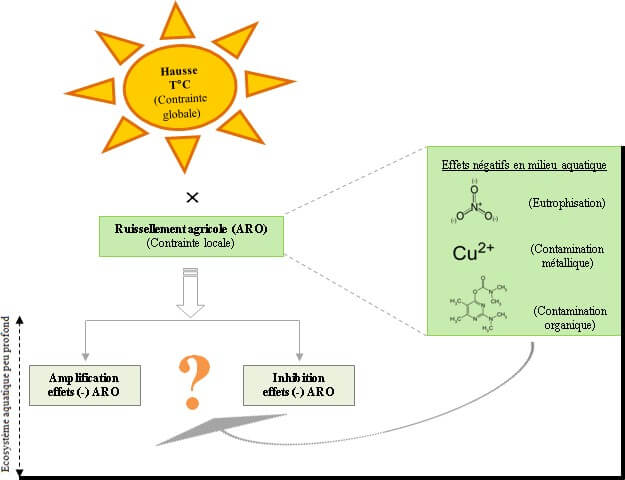
Figure 4: Conceptualisation des effets combinés de stress en milieux aquatiques peu profonds ARO = Agricultural Run-Off
1.3. Comportement et devenir des éléments provenant du ruissellement agricole dans les écosystèmes aquatiques peu profonds
1.3.1. Nitrate
Le nitrate est un anion polyatomique de formule chimique NO3-. Il est largement utilisé comme engrais azoté inorganique pour l’accroissement de la productivité agricole (Fried et al., 2003).
Bien qu’il soit un additif déterminant pour l’intensification de l’agriculture, il est aussi capable d’induire une perte drastique de la biodiversité aquatique (Douda, 2010).
En effet, le nitrate provenant des terres agricoles est capable de transiter par le biais des eaux de ruissellement pour atteindre les milieux aquatiques peu profonds en aval (Quin et al., 2015).
La présence d’un taux élevé de nitrate dans ces milieux conduit à leur eutrophisation (Spalding and Exner, 1993) ; (Spangler et al., 2019); entraînant de grandes variations du taux d’oxygène journalier. Ces conditions caractérisées pour la plupart du temps par une limitation en oxygène, font généralement suite à une perte drastique de la biodiversité aquatique (Moss et al., 2011).
C’est ce qui explique l’utilisation du nitrate comme additif dans la préparation du ruissellement agricole utilisé dans la présente étude.
1.3.2. Pesticides
D’un point de vue règlementaire, le mot « pesticide » désigne tous produits phytopharmaceutiques (encadrés par la Directive 91/414/CEE), comprenant les substances actives utilisées pour la prévention, le contrôle ou l’élimination d’organismes (plantes, animaux, champignons, bactéries) pouvant nuire au développement des cultures.
Ces produits peuvent être classés en fonction du type d’organisme qu’ils combattent. On distingue plusieurs types de pesticides. Ce sont entre autres les herbicides, les insecticides, les fongicides, les rongicides et les vermicides), tous sont nuisibles pour les organismes aquatiques.
Au nombre de ces derniers, les plus utilisés sont les herbicides, insecticides et fongicides. Ils ont été respectivement représentés dans cette étude par :
– la Terbuthylazine (C9H16CIN5), appartenant à la famille chimique des triazines (C3H3N3).
C’est un herbicide très utilisé en agriculture pendant la croissance des cultures (Schreiner et al., 2016).
Il agit en tant qu’inhibiteur de la photosynthèse des macrophyte du genre Lemna mais a également été signalée toxique pour les invertébrés aquatiques en affectant par exemple l’abondance de Daphnia magna exposés à une dose sublétale de 3 µg.L-1 (Barmentlo et al., 2018) et en entraînant la mortalité de Scrobicularia plana exposés à des doses létales allant de 40 mg.L-1 à 138 mg.L-1 (Gutiérrez et al., 2019) ;
– le Pirimicarb (C11H18N4O2), appartenant à la famille chimique des carbamates. Egalement très utilisé en agriculture pour son effet insecticide sur les plantes terrestres.
Une exposition à des concentrations environnementales de ce toxique, peut inhiber l’activité bactérienne dans les communautés microbiennes des sédiments.
L’exposition aux pesticides testés peut donc induire des réactions toxiques dans les communautés microbiennes des sédiments à des concentrations présumées sans danger pour l’environnement (Widenfalk et al., 2009).
Il peut aussi agir négativement sur la croissance et sur les paramètres de reproduction de D. magna exposé à des pulses répétés de 70 µg.L-1 (Andersen et al., 2006) et sur le système nerveux de Lymnaea stagnalis en agissant sur le métabolisme de la polyamine impliquée dans les lésions du système nerveux central de l’animal (Tufi et al., 2016) ;
– le Tébuconazole (C16H22ClN3O) appartenant à la famille chimique des triazoles. Il sert de fongicide agissant notamment sur les champignons ravageurs des plantes en s’attaquant à leurs spores ou à leur perméabilité membranaire.
Quand il se retrouve en milieux aquatiques, il peut provoquer une diminution du taux de croissance spécifique et une perturbation du métabolisme énergétique chez le macrophyte Bidens laevis ((Moreyra et al., 2019).
Une étude récente de Bruno KenjiOrtiz-Cañavate et al. (2019) a montré que bien qu’étant toxique, lorsqu’il est appliqué en mélange à une dose de 200 μg.L-1, il peut favoriser la prolifération de cyanobactéries toxiques. En revanche, il induit des effets négatifs tant sur la survie que sur la croissance des individus de D. magna exposés à une dose de 0,41 mg.L-1.
Globalement, les pesticides constituent un énorme progrès pour l’agriculture moderne, en augmentant les rendements de production.
Cependant, depuis quelques années, ces produits sont soumis à une réglementation beaucoup plus endurcies étant donné leur potentiel toxique sur les différents compartiments environnementaux. Leur présence est donc de plus en plus surveillée.
C’est pour ces raisons qu’ils ont servi à reproduire le ruissellement agricole utilisé dans la présente étude.
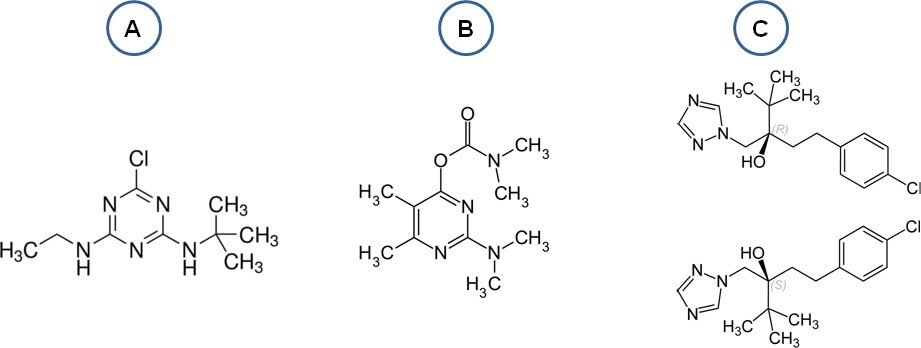
Figure 5: Structures complètes des substances actives de pesticides utilisées dans le cadre de l’étude. A = Terbuthylazine, B = Pirimicarb et C = Tébuconazole
1.3.3. Cuivre
Naturellement présent dans la croute terrestre, à faible dose, le cuivre (Cu) est un élément chimique essentiel au développement de toute forme de vie.
C’est un métal de transition, rouge- brun, malléable et ductile, excellent conducteur électrique et thermique. Il a pendant des siècles été utilisé comme un matériau de base de l’industrie électrique et de la construction.
De part ses caractéristiques (fongicide, algicide, bactéricide et herbicide) son utilisation aujourd’hui s’étend à plusieurs domaines dont celui de l’agriculture où il sert notamment d’additif « bouillie bordelaise » pour la protection des cultures contre les fongiques (Borkow and Gabbay, 2005).
La préparation de l’additif se fait à base d’un mélange de sulfate de cuivre et de chaux.
Sous l’effet du ruissellement de sols contaminés, le cuivre provenant des terres agricoles échoue dans les milieux aquatiques peu profonds à des concentrations supérieures à 20 ppb (Rainbow, 2002) affectant généralement la croissance des macroalgues (Geddie and Hall, 2019) et le taux de croissance des individus de Dreissena polymorpha via un faible taux de filtration (Kraak, 1997).
Ces constats font partie des raisons qui motivent le choix de cet élément trace comme additif dans la préparation du ruissellement agricole utilisé dans cette étude.
1.3.4. Toxicité des mélanges de polluants : additivité, synergie et antagonisme
En mélange, les effets toxiques de chaque polluants pris individuellement peuvent s’additionner ou non. Dans ce dernier cas, on parle d’interaction.
Plusieurs types d’interactions possibles existent et se traduisent généralement par la synergie ou l’antagonisme. Ces deux potentiels d’interactions complexes entre de multiples facteurs de stress constituent l’une des plus grandes incertitudes pour la prévision des changements écologiques (Darling et al., 2010).
La synergie est utilisée pour définir l’effet cumulatif de plusieurs facteurs de stress supérieur aux effets attendus en additionnant les effets individuels. En revanche, le terme antagonisme s’utilise lorsque l’effet combiné des deux stress chimiques est inférieur à la somme des effets individuels (Piggott et al., 2015b) .
1.4. Utilisation des microcosmes en évaluation du risque
Par définition, les bioessais monospécifiques permettent d’étudier les effets des contaminants au niveau individuel, mais pas aux niveaux d’organisations biologiques supérieurs (Forbes and Galic, 2016).
Cette méthode est source d’incertitudes liées principalement à l’extrapolation spatio- temporelle (du laboratoire au terrain et de la toxicité à court terme à une toxicité à long terme).
Cependant, à l’opposé des tests monospécifiques, les approches en « cosmes » (micro, méso et macrocosmes) beaucoup plus complexes, apparaissent comme un compromis intéressant permettant de réaliser des études d’évaluation de risques écotoxicologiques à différents niveaux d’organisations biologiques (Clement et al., 2014).
Par exemple, on retrouve au sein des dispositifs en « cosmes » les fonctions biologiques et les interactions majeures caractéristiques d’un écosystème (Figure 6). C’est la production primaire brute, la respiration de l’écosystème, le recyclage des éléments ou la dégradation de la matière organique, la prédation, la compétition et la reproduction.
Puisque l’évaluation des risques liés aux contaminations dans les écosystèmes peu profonds implique une prise en compte optimale des interactions biotiques qui influencent les fonctions écosystémiques (Lamonica, 2016). Alors, comparés aux autres types de dispositifs en « cosmes », les microcosmes de laboratoire présentent une simplicité et une répétabilité plus élevées.
Ils constituent par conséquent un outil adéquat pour l’évaluation du risque en écotoxicologie quand il s’agit bien sûr d’aller au-delà d’un seul niveau d’organisation.
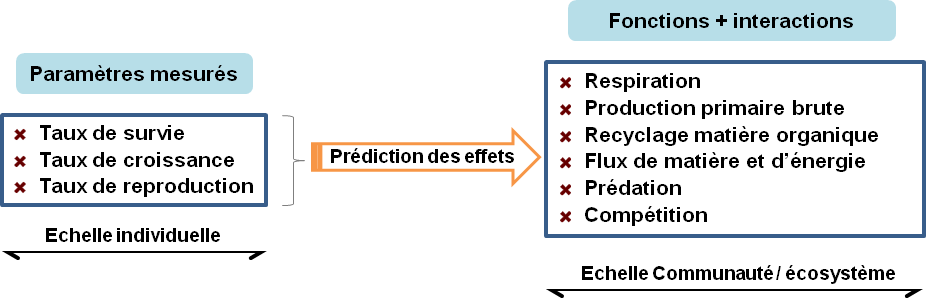
Figure 6: Représentation schématique de quelques paramètres, interactions et fonctions biologiques échelles individuelles, communautaires et écosystémique) pouvant être mesurés dans un microcosme pour une évaluation des risques écotoxicologiques
1.5. Biocénose des microcosmes
Les organismes utilisés pour l’étude en microcosme occupent chacun une place de choix dans la dynamique et le fonctionnement des milieux aquatiques peu profonds.
Ils ont déjà fait l’objet de bioessais monospécifiques et couvrent les principaux niveaux trophiques. Ce sont les producteurs primaires (phytoplancton, périphyton et macrophyte) et les consommateurs primaires (zooplancton, moule et mollusque gastéropode).
Parmi tous ces organismes, seuls les consommateurs primaires ont servi de modèles biologiques pour la présente étude. Il s’agit notamment de :
– Daphnia magna (Straus, 1820), cladocère d’eau douce mesurant 1,5 à 5 mm de longueur. Elle se retrouve typiquement inféodée dans les milieux pélagiques où elle joue un rôle clé de voute (Nilssen and Waervågen, 2002).
Elle exerce non seulement un contrôle ascendant ou encore « Top down » sur les communautés de phytoplancton (Degans and Meester, 2002) mais elle sert aussi de nourriture pour les poissons (juvéniles et adultes).
Cette espèce a été choisie par la présente étude pour : (1) sa visibilité à l’œil nu, (2) son taux de fécondité très élevé (3) son élevage relativement simple à réaliser (4) son cycle de vie court, et (6) sa sensibilité remarquable à une large gamme de produits chimiques (Parolini et al., 2018).
Elle fait aussi l’objet de tests aigus et chroniques normalisés (Versteeg et al., 1997) inscris dans la ligne directive de l’Organisation de Coopération et de Développement Economique (OCDE N°211 : tests aigus et OCDE N°214 : tests chroniques) ;
– Lymnaea stagnalis (Linnaeus, 1758), gastéropode d’eau douce qui mesure jusqu’à 5 à 6 cm de longueur. Largement répandu dans toute l’Europe, en Asie du Nord et en Amérique du Nord, L. stagnalis est un herbivore qui a une affinité pour les eaux lentes et fraîches avec des substrats sableux et vaseux (Amorim et al., 2019).
Il semble s’épanouir aux alentours de 24 ° C en montrant une survie et une production d’œufs maximales. C’est également un organisme clé du régime alimentaire de nombreuses espèces de consommateurs secondaires (poissons, écrevisses, amphibiens, mammifères et oiseaux.
Par conséquent, il joue un rôle crucial dans le fonctionnement et la santé des nombreux écosystèmes aquatiques (Segner et al., 2003). Il sert de modèle biologique utilisé en écotoxicologie du fait de son mode de reproduction (hermaphrodite) et de sa capacité de bioaccumulation élevée (Hudson et al., 2019).
C’est d’ailleurs l’une des deux espèces retenues avec Potamopyrgus antipodarum, pour l’élaboration d’une ligne directrice de l’OCDE (OCDE N°243) concernant le test de reproduction chez les mollusques (Matthiessen, 2008) ;
– Dreissena polymorpha (Pallas, 1771), ou « moule zébrée » est un bivalve invasif appartenant à la famille des Dreissenidae et mesurant 0,5 à 5 cm de longueur.
C’est un organisme typiquement inféodé aux milieux d’eaux douces avec des températures allant jusqu’à 30°C (Aldridge et al., 1995). Tout comme les consommateurs suscités, la moule zébrée est également une source de nourriture essentielle pour plusieurs poissons indigènes (Simberloff and Holle, 1999).
Sa biologie est caractérisée par un mode de vie sessile, une nutrition par filtration (capacités digestives de phagocytose et d’endocytose très développées) et un grand effort de reproduction.
Outre ces propriétés principales, ses caractéristiques spécifiques (potentiel d’accumulation élevé, large répartition géographique et acquisition à moindre coût) lui confèrent des avantages indéniables dans les études écotoxicologiques (Guerlet et al., 2007) ; (Louis et al., 2019)
Evaluation des facteurs de réponse des consommateurs aquatiques modèles exposés à de multiples facteurs de stress
Rapport de stage Master 2ème année Année 2018-2019
Mention Gestion de l’environnement (GESTE) Spécialité Ecologie, Ecotoxicologie
