La technique 5 champs et le cancer du nasopharynx
La technique 5 champs
Evaluation dosimétrique des techniques de traitement pour le cancer du nasopharynx
En radiothérapie conformationnelle 3D, il existe différentes techniques de traitements mais deux sont les plus utilisés, la technique classique et la technique à 5 champs qu’on va les détailler précisément dans la suite.
I. Matériels et méthodes
I.1 Matériels
Echantillonnage
L’échantillon se compose d’une série des 3 patients, 2 femmes, et un homme, d’Age moyen de 37 ans et de classification différente.
Scanner dosimétrique et moyen de contention :
Nous avons construit des plans de traitement en radiothérapie conformationnelle tridimensionnelle (RTC-3D) en utilisant d’abord un scanner simulateur General Electric® et avec un masque thermoformé à 3 points pour la reproductibilité du même positionnement, intégrés dans le Centre Régional d’Oncologie.
Fig 3.1 : Scanner simulateur.

Fig 3.2 : Masque thermoformé 3 points.
Système de planification de traitement
La planification du traitement a été effectuée à l’aide d’un TPS Eclipse® basé sur l’algorithme Pencil Beam Convolution qui permet de calculer la dose avec la correction de densité tissulaire., conformément aux procédures habituelles du Service. Cela concerne le nombre de faisceaux, leurs orientations, les pondérations et les accessoires.
Contourage des volumes irradiés et des organes à risque
C’est un acte purement médical, pour les tumeurs du Nasopharynx, outre la protection de la moelle épinière est primordiale ici.
GTV, CTV : ils sont déterminés d’après l’extension tumorale (en fonction des données cliniques, de l’endoscopie ORL, de l’imagerie, du compte rendu anatomopathologique), en tenant compte de l’histoire naturelle de la maladie.
PTV : les marges de sécurité sont déterminées en fonction des mouvements internes des volumes et de la technique de repositionnement utilisée (contentions, repères…).
Inclusion des aires ganglionnaires rétro pharyngées dans les volumes cibles anatomocliniques.
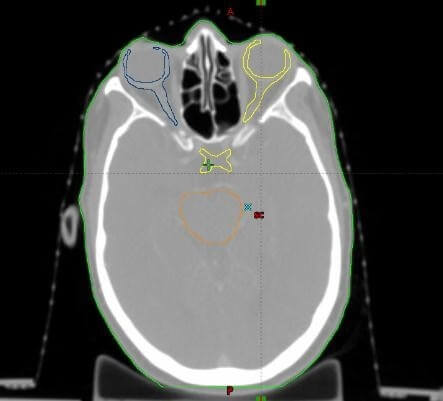
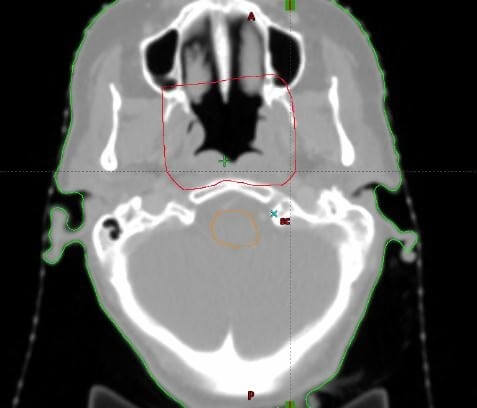
Fig 3.3 : Contourage des volumes cibles (rouge) , et OAR (bleu, jaune orange).
I.2 Méthodes
Techniques et balistiques de traitement
Les faisceaux sont définis et positionnés en simulation virtuelle à l’aide du Beam Eye View (BEV), pour chaque angulation on tient en compte les organes à risque qui sont colorés et entourés en volume.
Lors de la définition des faisceaux dans la salle de dosimétrie, l’effort maximum est fait pour éliminer toute focalisation possible, d’un faisceau à un organe à risque.
Pour bien comprendre la localisation des faisceaux par rapport au positionnement des organes à risques, une image numérique de chaque champ simulé peut être obtenue à l’aide du positionnement de ce dernier par rapport à DRR (Digitally Reconstructed Radiograph).
Description des techniques et balistiques de traitement Technique classique
Le patient est en décubitus dorsal avec un masque thermoformé 3 points et cale tête.
| Champ | Energie (MV) | Pondération | Rotation Bras | Rotation Colli |
| Latéral droit | X̴ 6 | 1.00 | 270.00° | 357.00° |
| Latéral gauche | X̴ 6 | 1.00 | 90.00° | 3.00° |
| Latéral droit (Reduction1) | X̴ 6 | 1.00 | 270.00° | 357.00° |
| Latéral gauche (Reduction1) | X̴ 6 | 1.00 | 90.00° | 3.00° |
| Latéral droit (Reduction2) | X̴ 6 | 1.00 | 270.00° | 357.00° |
| Latéral gauche (Reduction2) | X̴ 6 | 1.00 | 90.00° | 3.00° |
| Sc | X̴ 6 | 1.00 | 0.00° | 0.00° |
Tab 3.1 : Description des champs dans la technique classique.
Cette technique consiste à irradier le PTV50 par deux champs latéraux opposés 90° et 270° avec une rotation de collimateur dans le latéral gauche 3°, le latéral droit 357° et d’énergie Photons – 6 MV.
Dans la 1ère série :
En 1er temps par une dose de 40 Gy, avec 2 Gy/ séance, 5 jours / semaine, dans la partie supérieure du PTV50, en conservant le tronc cérébral, le nerf optique et les autres OARs.
Puis en 2éme temps par un dose de 10 Gy dans le PTV50 aussi, mais en cachant la moelle épinière (Plan de Reduction).
En 3éme temps par une dose de 20 Gy dans le PTV 70, Après, on a irradié la partie susclave (la partie inférieure du PTV50) par une dose de 50Gy avec un champ antérieur tout en cachant la moelle épinière.
Dans la 2éme série, ce qui concerne les parties cachées du PTV50, elles sont irradiées par des champs latéraux opposés par des faisceaux d’électrons par une dose de 10 Gy pour que le PTV50 reçoit 50 Gy en total, traités en DSP = 105-110, cet éloignement est nécessaire pour éviter le contact entre l’applicateur des électrons et les épaules. Avec les mêmes angulations du bras et collimateur.
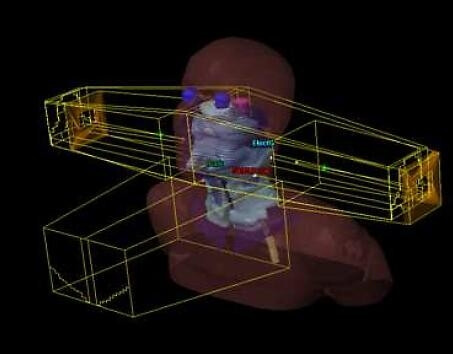
Fig 3.4 : Illustration de l’ensemble des faisceaux de la technique classique.
Technique 5 champs
Le patient est en décubitus dorsal avec un masque thermoformé 3 points et cale tête.
La technique est basée que sur l’irradiation avec les faisceaux des photons, y’a pas d’utilisation des électrons.
L’irradiation est faite par 5 champs, 2 latéraux opposés et un antérieur :
| Champ | Energie (MV) | Pondération | Rotation Bras | Rotation Colli |
| Latéral droit | X̴ 6 | 0.40 | 270.00° | 90.00° |
| Latéral gauche | X̴ 6 | 0.40 | 90.00° | 90.00° |
| Postérieur | X̴ 18 | 0.04 | 180.00° | 90.00° |
| Oblique post droite | X̴ 18 | 0.08 | 223.00° | 0.00° |
| Oblique post gauche | X̴ 18 | 0.08 | 140.00° | 0.00° |
| Latéral droit (Reduction) | X̴ 6 | 1.00 | 270.00° | 0.00° |
| Latéral gauche (Reduction) | X̴ 6 | 1.00 | 90.00° | 0.00° |
| Sc | X̴ 6 | 1.00 | 0.00° | 0.00° |
Tab 3.2 : Description des champs dans la technique 5 champs.
Une dose de 50 Gy dans le PTV50, avec 2 Gy/ séance, 5 jours / semaine avec plan de 5 champs. Puis une dose de 20 Gy est délivrée au PTV70 avec deux champs latéraux opposés.
Et finalement la partie sus clave, 50 Gy avec un champs antérieur.
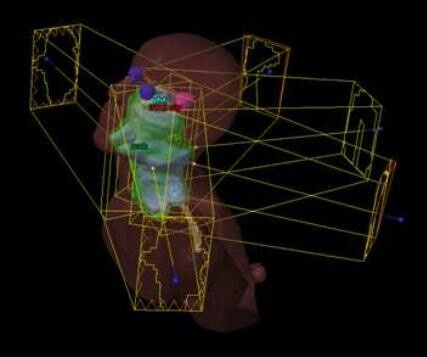
Fig 3.5 : Illustration de l’ensemble des faisceaux de la technique 5 champs.
Dans cette partie pratique concernant les deux techniques, on a choisi chaque champ individuellement, nous avons fait l’optimisation du MLC à la structure du volume PTV d’une manière automatique avec une distance bien définit, où le choix de cette distance est de respecter la pénombre du profil de la dose pour bien entourer le volume cible PTV par la dose prescrite. Cependant, on augmente cette distance dans les parties concaves de la tumeur.
De plus, nous avons fait la création d’un point de référence de dose, son rôle est d’administrer la dose dans le volume cible prévisionnel entre 95 % et 107 %.9
[13][Jean-Philippe et al.] : Jean-Philippe, et al. Guide des technologies de l’imagerie médicale et de la radiothérapie Quand la théorie éclaire la pratique Illustrations, dillenseger Préface à la 2e édition Jean-Louis dietemann 2e édition.
[14][Da Deconto] : SPIM , thèse de doctorat , évaluation dosimétrique des algorithmes implémentés dans les TPS en présence d’hétérogénéité de forte densité . cas de la sphère ORL en RTE.
[15][SFPM]: Guide des bonnes pratiques de physique médicale SOCIÉTÉ FRANÇAISE DE PHYSIQUE MÉDICALE (SFPM, EDP ).
[16][SFPM] : Recommandations pour la mise en service et l’utilisation d’un système de planification de traitement en radiothérapie (TPS)par SFPM 2010.
[16.Bis][J. Chavaudra et al.] : J. Chavaudra, A. Bridier. Définition des volumes en radiothérapie externe : rapports ICRU 50 et 62 Service de physique, institut Gustave-Roussy, 94805 Villejuif cedex.
[17] : » www.sante-sur-le-net.com/maladies/examens-medicaux/radiotherapie/ «.
[18][Holder allen et al.] : Holder Allen, et al. A tutorial on radiation oncology and optimization [Article] .Mathematics Faculty Research.
[19][Harald Paganetti] : [Medical Physics and Biomedical Engineering volume 20] Harald Paganetti – Proton Therapy Physics (2011, Taylor and Francis)
[20][Arfaoui et al.] : Le cancer du cavum au Maroc. Etude épidémiologique sur l’échantillon: Centre d’oncologie Al Azhar de Rabat, Arfaoui et al., 2007. Antropo.
Contraintes de dose
Les organes à risque sont : les parotides ; le tronc cérébral, la moelle ; le nerf optique, le chiasma, la jonction temporomandibulaire, le conduit auditif externe et interne, la mandibule, l’œil , le cristallin, le cerveau (lobe temporal), (la peau ; la langue mobile ; le larynx pour les lésions avec atteintes cervicales ganglionnaires basses).
Ces organes ont des contraints de dose qu’on ne doit pas les dépasser.
Les données répertoriées dans le tableau (3.1) sont issues du Guide des procédures en radiothérapie externe 2007, en fractionnement de 2 Gy, à raison de 5 séances par semaine.
| Organe | Contrainte(s) |
| Cerveau (lobe temporel) | Dmax : 60 Gy |
| Parotide controlatérale | V26<50% , Dmoyenne < 30 Gy |
| Parotide homolatérale | Dose la plus basse possible |
| Articulation temporomandibulaire | Dmax : 65 Gy |
| Larynx sain | Dmoyenne < 43.5 |
| Oreille interne | Dmax : 60 Gy |
| Cochlée | Dmax : 58 Gy |
| Tronc cérébrale | Dmax < 54 Gy Dmax = 64 Gy (surface) . |
| Nerf optique, chiasma | Dmax < 54 Gy |
| Moelle épinière cervicale | Dmax<50 Gy , Si association chimioradiothérapie Dmax<45 Gy |
| Œil | Dmoyenne < 35 Gy |
| Cristallin | Dose <10 -15 Gy |
Tab 3.3 : Contraintes de dose pour les OARs. [3]
[1][Maryse Delehedde] : Maryse Delehedde -Que sait-on du cancer _-EDP SCIENCES (2006)
[2][W.Schlegel et al.] : W.Schlegel, T.Bortfeld, A.-L.Grosu , MedicNew Technologies in Radiation Oncology (2006, Springer)
[2.Bis][Herrassi et al.] : Herrassi MY, Bentayeb F, Malisan MR. Comparative study of four advanced 3d-conformal radiation therapy treatment planning techniques for head and neck cancer. J Med Phys [serial online] 2013 [cited 2019 Mar 27];38:98-105.
[3][B.Fleury el al.] : B.Fleury, M.C. Biston, X.Montarbon, P. Pommier , Cancers du cavum de l’adulte , Cancer Radiotherapie , ELSEVIER .
Analyse dosimétrique
De nombreux indices sont proposés dans la littérature pour compléter ces évaluations. Nous allons voir deux types d’indices au sujet des différents volumes d’intérêt : indice d’homogénéité et l’indice de conformation pour le volume cible (PTV).
ICRU a recommandé un indice appelé Homogeneity Index (HI) pour déterminer l’homogénéité globale de la dose absorbée par le PTV [28]
Il est défini comme indiqué ci-dessous :
𝑯𝑰(𝑹𝑪𝟑𝑫) = 𝑫𝒎𝒂𝒙−𝑫𝒎𝒊𝒏
𝑫𝒎𝒐𝒚
(3.1)
Une valeur très proche de 0 implique que la dose déposée dans le PTV est quasi homogène.
L’objectif d’optimisation est de faire décroitre l’indice vers la valeur idéale de 0.
Le Radiation Therapy Oncology Group (RTOG) a élaboré un index appelé « Conformation Index » (CI) pour déterminer la couverture du PTV par l’isodose de référence ( (ICRU 50, 1993) a recommandé comme isodose de référence)) : Il est défini comme indiqué ci-dessous :
𝑽𝑷𝑻𝑽
𝟗𝟓%
𝑽𝑷𝑻𝑽
(3.2)
𝑽𝑷𝑻𝑽 Représente le volume couvet par l’isodose 95% de la dose prescrite au PTV.
𝑽𝑷𝑻𝑽 Représente le volume du PTV
La valeur idéale de CI est de 1, L’objectif d’optimisation est de faire croitre l’indice vers la valeur idéale de 1.
Par indices biologiques
1. Model gEUD (generalized Equivalent Uniform Dose) :
La définition originale de l’gEUD a été dérivée sur la base d’une formulation mécaniste utilisant un modèle de survie cellulaire linéaire et quadratique calculée à partir d’un histogramme dose volume différentiel.
𝒂 𝟏
g𝑬𝑼𝑫 = (∑𝒊=(𝑽𝒊𝑫𝒊 ) )𝒂 (3.5)
𝑎 : est un paramètre de modèle sans unité qui est spécifique à chaque structure normale ou de la tumeur d’intérêt.
𝑉𝑖 = 𝑣𝑖 (sans unité) , qui présente le iém volume partiel recevant la dose Di en Gy .
Pour cette raison, puisque le volume relatif de toute la structure d’intérêt correspond à 1, la somme de tous les volumes partiels vi sera égale à 1.
Les paires de données Di et 𝑣𝑖 sont obtenues à partir de l’HDV différentielle non cumulatif d’un plan de radiothérapie donné.
Le choix de 𝑎 déterminera le comportement du modèle basé sur l’EUD :
• Si 𝑎 prend un grand nombre positif, EUD est proche de la valeur maximale de la dose.
• Si 𝑎 prendre un nombre négatif, EUD est proche de la valeur minimale de la dose.
• Si 𝑎 est égal à 1, EUD devient la dose moyenne.
2. NTCP (Normal Tissue Complications Probability)
NTCP basé sur gEUD
Pour calculer la probabilité de complication tissulaire normale basée sur l’gEUD, nous utilisons la fonction logistique :
𝑵𝑻𝑪𝑷 = 𝟏
𝟏+ (𝑻𝑫𝟓𝟎
𝟒𝜸𝟓𝟎
(3.6)
𝑬𝑼𝑫 )
Avec : 𝑇𝐷50 est la dose de tolérance pour un taux de complication de 50% à un intervalle de temps spécifique (par exemple 5 ans dans les données de tolérances tissulaires normales) lorsque le patient est irradié de manière homogène.
𝛾50: est un paramètre de modèle sans unité spécifique à la structure normale, qui décrit la pente de la courbe dose-réponse.
NTCP du model de Lyman
Ce modèle permet de comparer les plans de traitement de point de vue de la complication des OARs.
𝑵𝑻𝑪𝑷 = 𝟏
√𝟐𝝅
𝟐
−∞ 𝐞𝐱𝐩 (− 𝟐 ) 𝒅𝒙
(3.7)
𝑡 = 𝐷−𝑇𝐷50(𝜗)
𝑚∗ 𝑇𝐷50(𝜗)
(3.8)
𝑇𝐷50(1) = 𝑇𝐷50(𝜗) ∗ 𝜗𝑛 (3.9)
𝜗 = 𝑉
𝑉𝑟𝑒𝑓
(3.10)
Où les 4 paramètres du modèle sont : 𝑉𝑟𝑒𝑓, 𝑇𝐷50 , 𝑛 , 𝑚 . sont donnés par [Emami et al.]
• 𝑉𝑟𝑒𝑓 : Est le volume de référence.
• 𝑇𝐷50(𝜗) : Est la dose de tolérance pour une probabilité de complication de 50% pour irradiation uniforme du volume partiel 𝜗.
• 𝑇𝐷50(1) : Est la dose de tolérance pour une probabilité de complication de 50% pour irradiation uniforme du volume entier.
• 𝑛 ∶ Détermine la dépendance en volume de la probabilité de complication de complication
• 𝑚 : Est un caractère propre à chaque tissu.
Pour déterminer la valeur de NTCP, on doit utiliser l’histogramme dose volume cumulatif de l’organe étudié, le volume est décomposé en volume effectif.
2. TCP (Tumor Control Probability)
Pour calculer la probabilité de contrôle de la tumeur basée sur l’EUD.
𝑻𝑪𝑷 = 𝟏
𝟏+ (𝑻𝑪𝑫𝟓𝟎
𝟒𝜸𝟓𝟎
(3.9)
𝑬𝑼𝑫 )
Avec : 𝑇𝐶𝐷50: La dose pour contrôler 50% des tumeurs, lorsque la tumeur est irradiée de manière homogène.
Ces indices biologiques vont être calculer à l’aide d’un programme C++. [voir l’ANNEXE]
Analyse clinique
Afin de vérifier que le plan de traitement satisfait au mieux les contraintes médicales préétablies, des évaluations qualitatives et quantitatives de la distribution de dose sont nécessaires.
D’un point de vue qualitatif, l’évaluation des courbes isodoses est couramment utilisée. Elles permettent de visualiser la conformation de la dose au volume cible et de localiser des régions de surdosage ou sous-dosage.
D’un point de vue quantitatif, l’évaluation de l’histogramme dose volume (HDV) est envisagée. Un HDV comprend généralement l’ensemble des structures (volumes cibles et organes à risque) et des objectifs d’intérêt dans le plan de radiothérapie, chaque courbe représente une structure spécifique.
Chaque point d’une courbe représente le pourcentage en volume de la structure associée recevant une dose au moins égale à la dose lue en abscisse.
Un HDV de la tumeur serait idéalement une fonction en échelon, avec 100% de la cible recevant exactement la dose prescrite et 0% recevant plus. Un HDV idéal de la structure critique serait une fonction avec 100% du volume de la structure recevant 0% de la dose prescrite.
Un HDV capture les informations volumétriques qui sont difficiles à percevoir à partir des courbes d’isodoses.
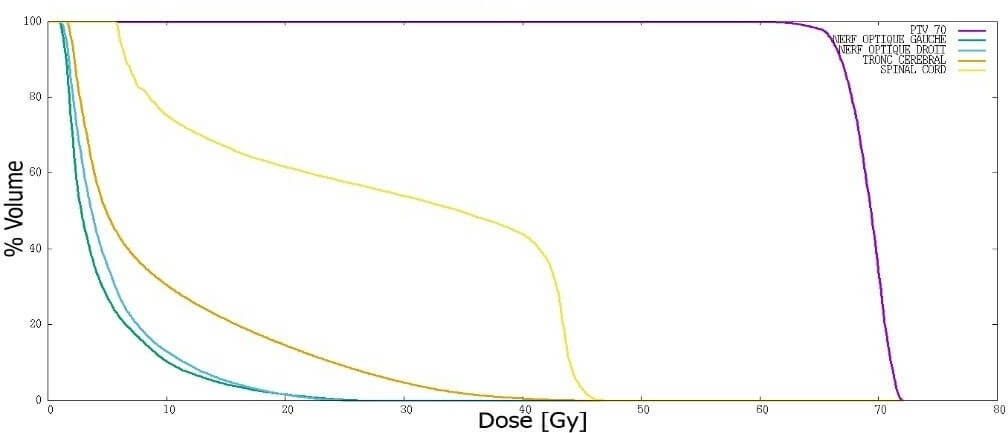
Fig 3.6 : Histogramme Dose Volume (HDV).
II. Résultats et discussion
Résultats
L’objectifs de cette partie du travail est de comparer les deux techniques, classique et 5 champs pour le traitement du Nasopharynx, en prenons deux modèles, il s’agit de deux patients atteints d’un cancer du Nasopharynx et traités au service de radiothérapie de Centre Régional d’oncologie.
Quel que soit l’indication de la radiothérapie, la problématique essentielle étant de minimiser le maximum possible les séquelles et les complications par une technique rigoureuse en respectant les organes critiques. La base de la technique d’irradiation est la même, ce qui varie sont les volumes cibles traités ainsi que les doses délivrées.
Le physicien détermine la balistique en vérifiant la distribution de dose au niveau des volumes cibles PTV définit par le médecin ainsi que les doses de tolérance de chaque organe à risque. Le principal but de la dosimétrie consiste à avoir une optimisation meilleure sur les volumes cible en épargnant les organes à risque.
[4][Ching-yeh Hsiung et al.] : CHING-YEH HSIUNG, M.D et al. INTENSITY- MODULATED RADIOTHERAPY VERSUS CONVENTIONAL THREE-DIMENSIONAL CONFORMAL RADIOTHERAPY FOR BOOST OR SALVAGE TREATMENT OF NASOPHARYNGEAL CARCINOMA,Int. J. Radiation Oncology Biol. Phys., Vol. 53, No. 3, pp. 638–647, 2002 , ELSEVIER
[5][Yann Perrot] : Yann Perrot. Evaluation de la dose déposée par des faisceaux d’électrons en radiothérapie dans des fantômes voxelisés en utilisant la plateforme de simulation Monte Carlo GATE fondée sur GEANT4 dans un environnement de grille. Autre [cond-mat.other]. Université Blaise Pascal – Clermont-Ferrand II, 2011. Français.
[6][e-cancer] : » www.e-cacncer.fr » .
[7][INSTN] : INSTN , Personne competente en radioprotection . Principes de radioprotection – Christine Jimonet, Henri Métivier.
[8][Henri Metivier] : Henri Metivier , Genie atomique , Radioprotection et ingenieurie nucleaire ( L’Editeur _ EDP Sciences).
[9][Walter & Miller] : Radiotherapy_ Radiation Physics, Therapy and Oncology-Churchill Livingstone (2012).
[10][AIEA] : International Atomic Energy Agency «Radiation oncology physics: a handbook for teachers and students», ISBN 92–0– 107304–6 (Vienna, 2005).
[11][Daniel Blac] : DANIEL BLANC GUY PORTAL JEAN BARTHE «les rayonnements ionisants : détection, dosimétrie, spectrométrie» edition Dunod.
[12][Claude Le Sech]:Claude Le Sech, Christian Ngô-Physique nucléaire – Des quarks aux applications – Cours et exercices corrigés-Dunod (2014).
1st Patient
Analyse de la couverture des PTV à partir des dosimétries prévisionnelles
Sur les courbes isodoses, on trouve que l’isodose 95% (66.5 Gy) couvre 91.4% du PTV70 pour la technique classique et 96.7% pour la technique 5 champs.
Analyses des OAR et PTV à partir des HDV et calcule des indices
Les contraintes de dose au PTV et aux organes à risque sont les suivantes :
| Organe | Contrainte |
| Tronc cérébrale | Dmax < 54 Gy Dmax = 64 Gy (surface) . |
| Nerf optique, chiasma | Dmax < 54 Gy |
| Moelle épinière cervicale | Dmax<50 Gy , Si association chimioradiothérapie Dmax<45 Gy |
| Œil | Dmoyenne < 35 Gy |
| Cristallin | Dose <10 -15 Gy |
Tab 3.4 : Les contraintes de dose pour les OARs.
Technique classique
La dose minimale reçue par le PTV70 est de 53.537 Gy et la dose maximale est de 75.033 Gy. Les contraintes au niveau de la moelle, l’Œil, les nerfs optiques et le tronc cérébrale sont respectées.
A partir des données mesurées en C.R.O, les volumes, les doses moyennes minimales, maximales délivrées aux organes à risque et au PTV sont résumées dans le tableau suivant :
| Organe | Volume [cm3] | Dmax[Gy] | Dmin [Gy] | Dmoy [Gy] |
| PTV70 | 99.200 | 75.033 | 53.537 | 69.434 |
| Chiasma | 1.800 | 2.803 | 2.213 | 2.513 |
| Nerfs optique droit | 0.500 | 2.681 | 1.603 | 2.031 |
| Nerfs optique gauche | 1.100 | 2.343 | 1.392 | 1.806 |
| Moelle épinière | 35.800 | 47.359 | 2.342 | 18.325 |
| Tronc cérébrale | 31.000 | 53.809 | 1.609 | 21.608 |
| L’Œil droite | 11.800 | 1.915 | 0.586 | 1.183 |
| L’Œil gauche | 10.500 | 1.548 | 0.548 | 0.969 |
| Cristallin droit | 0.200 | 0.912 | 0.710 | 0.818 |
| Cristallin gauche | 0.200 | 0.833 | 0.629 | 0.740 |
Tab 3.5 : Les différents résultats de la Dmoy ,Dmax ,Dmin et les volumes.
L’indice d’homogénéité
𝐻(𝑅𝐶3𝐷) = 𝐷𝑚𝑎𝑥 − 𝐷𝑚𝑖𝑛 = 75.033 − 53.537 = 0.309
𝐷𝑚𝑜𝑦
69.434
L’indice de conformité
𝑉𝑃𝑇𝑉
𝑉𝑃𝑇𝑉
302.200
99.200
= 3.044
| Organe | n | m | α | γ50 | TD50/5[Gy] | TCD50/5[Gy] |
| Tumeur | – | – | -8 | 2 | – | 72 |
| Moelle épinière | 0.05 | 0.175 | 7.4 | 4 | 66.5 | – |
| Tronc cérébrale | 0.06 | 0.14 | 4.6 | 3 | 65 | – |
Tab 3.6 : Les paramètres biologiques n,m,TD50/5 , TCD50/5 α et γ50 sont donnés par Emami et Al .[25]
| Organe | gEUD[Gy] | NTCPgEUD | NTCPLyman | TCPgEUD |
| Tumeur | 69.035 | – | – | 41.669% |
| Moelle épinière | 35.502 | 0.004% | 0.987% | – |
| Tronc cérébrale | 37.479 | 0.134% | 0.208% | – |
Tab 3.7 : Différente résultats de gEUD , NTCPLyman ,NTCPgEUD.
Technique 5 champs
La dose minimale reçue par le PTV70 est de 56.262 Gy et la dose maximale est de 74.042 Gy Ainsi que les contraintes au niveau de la moelle, l’Œil, les nerfs optiques et le tronc cérébrale sont respectées.
A partir des données mesurées en C.R.O, les volumes, les doses moyennes minimales, maximales délivrées aux organes à risque et au PTV sont résumées dans le tableau suivant :
| Organe | Volume [cm3] | Dmax[Gy] | Dmin [Gy] | Dmoy [Gy] |
| PTV70 | 99.200 | 74.042 | 56.262 | 70.023 |
| Chiasma | 1.800 | 2.710 | 2.262 | 2.497 |
| Nerfs optique droit | 0.500 | 2.602 | 1.842 | 2.204 |
| Nerfs optique gauche | 1.100 | 2.413 | 1.626 | 1.997 |
| Moelle épinière | 35.800 | 44.261 | 1.768 | 17.116 |
| Tronc cérébrale | 31.000 | 54.033 | 1.933 | 26.303 |
| L’Œil droite | 11.800 | 2.293 | 0.783 | 1.381 |
| L’Œil gauche | 10.500 | 1.929 | 0.804 | 1.271 |
| Cristallin droit | 0.200 | 1.167 | 0.983 | 1.065 |
| Cristallin gauche | 0.200 | 1.102 | 0.908 | 0.998 |
Tab 3.8 : Les différents résultats de la Dmoy ,Dmax ,Dmin et les volumes.
L’indice d’homogénéité
𝐻(𝑅𝐶3𝐷) = 𝐷𝑚𝑎𝑥 − 𝐷𝑚𝑖𝑛 = 74.042 − 56.262 = 0.253
𝐷𝑚𝑜𝑦
70.023
L’indice de conformité
𝑉𝑃𝑇𝑉
𝑉𝑃𝑇𝑉
297.900
99.200
= 3.303
| Organe | gEUD[Gy] | NTCPgEUD | NTCPLyman | TCPgEUD |
| Tumeur | 70.723 | – | – | 46.427% |
| Moelle épinière | 31.312 | 0.000% | 0.983% | – |
| Tronc cérébrale | 40.632 | 0.354% | 0.365% | – |
Tab 3.9 : Différente résultats de gEUD , NTCPLyman ,NTCPgEUD.
Comparaison des HDVs pour les 2 techniques
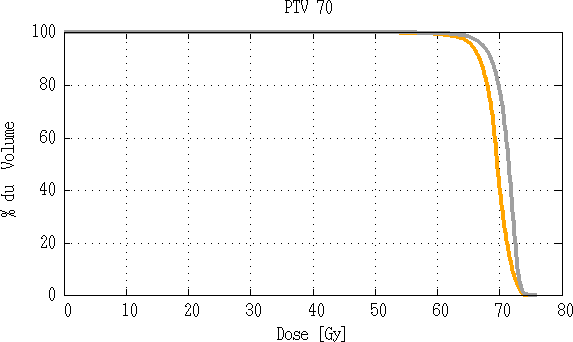
![]()
Fig 3.7 : Comparaison d’histogramme dose volume de le PTV70.
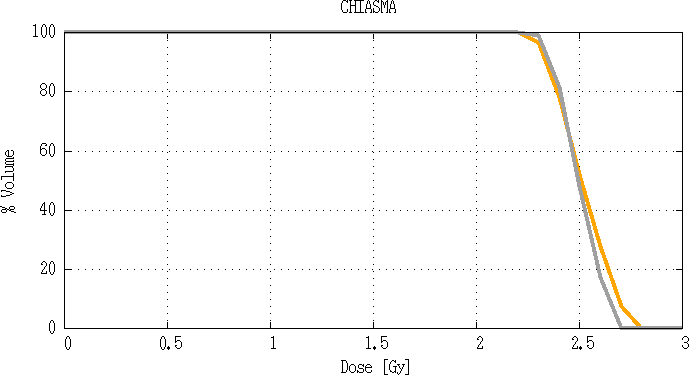
Fig 3.8 : Comparaison d’histogramme dose volume du chiasma optique
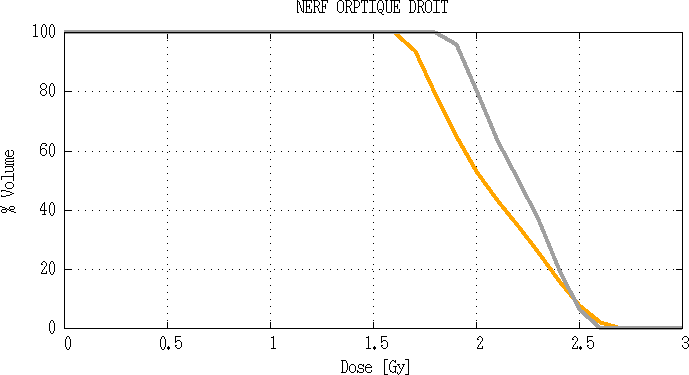
Fig 3.9 : Comparaison d’histogramme dose volume du nerf optique droit.
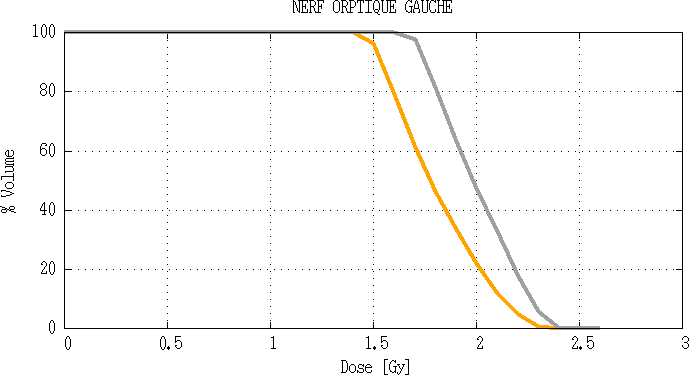
Fig 3.10 : Comparaison d’histogramme dose volume du nerf optique gauche.
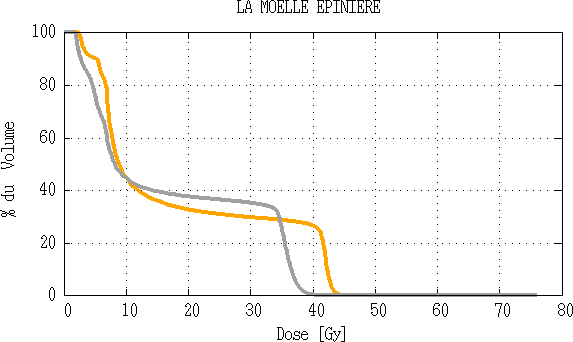
Fig 3.11 : Comparaison d’histogramme dose volume de la moelle épinière.
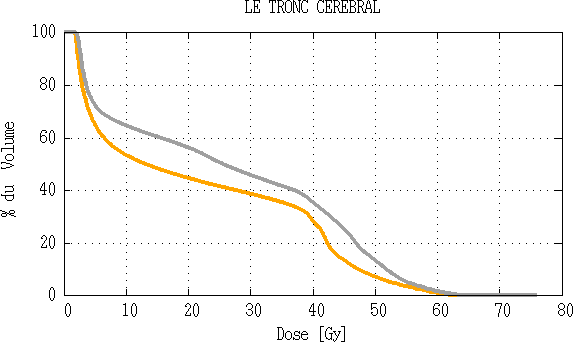
Fig 3.12 : Comparaison d’histogramme dose volume du tronc cérébral.
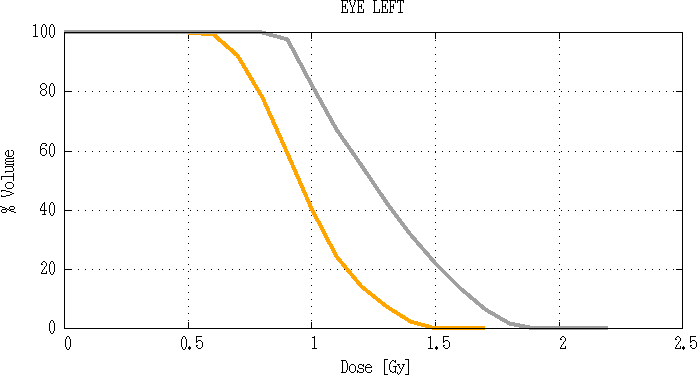
Fig 3.13 : Comparaison d’histogramme dose volume de l’œil gauche.
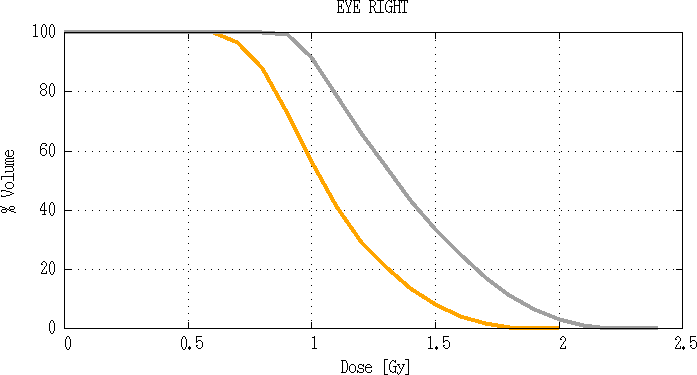
Fig 3.14 : Comparaison d’histogramme dose volume de l’œil droite.
2nd Patient
Analyse de la couverture des PTV à partir des dosimétries prévisionnelles
Sur les courbes isodoses en dosimétrie RC3D, on trouve que l’isodose 95% (66.5 Gy) couvre 84.1% du PTV70 pour la technique classique et 93.1% pour la technique 5 champs.
Analyses des OAR et PTV à partir des HDV et calcule des indices
[21][Madouri] : MADOURI Rachida. Place de l’association radiothérapie chimiothérapie concomitante (ARCC) dans la stratégie thérapeutique des cancers du cavum. Faculté de médecine Université D’ORAN.2012.
[22][Chua DT et al. ] : Chua DT, Sham JS, Kwong DL, Choy DT, Au GK, Wu PM. Prognostic value of para nasopharyngeal extension of nasopharyngeal carcinoma: a significant factor on local control and distant metastasis. Cancer 1996 Jul 15;78(2):202–10.
[22][Jean-Philippe Dillenseger] : Jean-Philippe Dillenseger (Auth.) – Atlas D’anatomie Générale et Radiologique-ELSEVIER-MASSON (2011).
[23][NCI] : National Cancer Institute. (2015, September 25). Nasopharyngeal Cancer Treatment (PDQ®) Health Professional Version. Extrait de: https://www.cancer.gov/types/head-and-neck/hp/nasopharyngeal-treatment-pdq#section/all.
[24][Edge SB el al.] : Edge SB, Byrd DR, Carducci MA, Compton CC, Fritz AG, Greene FL, et al. AJCC Cancer Staging Handbook: Springer-Verlag New York Inc.; 2009
[25][Emami et al.]:Emami B, Lyman J, Brown A, Coia L, Goitein M, Munzenrider JE, et al. Tolerance of normal tissue to therapeutic irradiation. Int J Radiat Oncol Biol Phys 1991;21:109–22
Technique classique
La dose minimale reçue par le PTV70 est de 45.953 Gy, et la dose maximale est de 76.251 Gy. Les contraintes au niveau de la moelle, l’Œil, les nerfs optiques et le tronc cérébrale sont respectées. A partir des données mesurées en C.R.O, les volumes, les doses moyennes minimales, maximales délivrées aux organes à risque et au PTV sont résumées dans le tableau suivant :
| Organe | Volume [cm3] | Dmax[Gy] | Dmin [Gy] | Dmoy [Gy] |
| PTV70 | 200.900 | 76.251 | 45.953 | 70.990 |
| Chiasma | 1.400 | 2.311 | 2.787 | 2.485 |
| Nerfs optique droit | 0.900 | 2.302 | 1.852 | 2.004 |
| Nerfs optique gauche | 1.000 | 2.113 | 1.736 | 2.197 |
| Moelle épinière | 37.900 | 45.290 | 0.451 | 10.942 |
| Tronc cérébrale | 24.800 | 54.017 | 2.764 | 34.434 |
| L’Œil droite | 8.100 | 32.010 | 1.037 | 4.217 |
| L’Œil gauche | 7.900 | 24.465 | 0.968 | 3.157 |
| Cristallin droit | 0.100 | 1.956 | 1.301 | 1.629 |
| Cristallin gauche | 0.100 | 1.991 | 1.229 | 1.577 |
Tab 3.10 : Les différents résultats de la Dmoy ,Dmax ,Dmin et les volumes.
L’indice d’homogénéité
𝐻(𝑅𝐶3𝐷) = 𝐷𝑚𝑎𝑥 − 𝐷𝑚𝑖𝑛 = 76.251 − 45.953 = 0.423
𝐷𝑚𝑜𝑦
L’indice de conformité
70.990
𝑉𝑃𝑇𝑉
𝑉𝑃𝑇𝑉
416.600
200.900
= 2.073
| Organe | gEUD[Gy] | NTCPgEUD | NTCPLyman | TCPgEUD |
| Tumeur | 69.293 | – | – | 46.396% |
| Moelle épinière | 31.241 | 0.000% | 0.823% | – |
| Tronc cérébrale | 41.761 | 0.492% | 0.836% | – |
Tab 3.11 : Différente résultats de gEUD , NTCPLyman ,NTCPgEUD..
Technique 5 champs
La dose minimale reçue par le PTV70 est de 52.855 Gy et la dose maximale est de 74.986 Gy. Les contraintes au niveau de la moelle, l’Œil, les nerfs optiques et le tronc cérébrale sont respectées. A partir des données mesurées en C.R.O, les volumes, les doses moyennes minimales, maximales délivrées aux organes à risque et au PTV sont résumées dans le tableau suivant :
| Organe | Volume [cm3] | Dmax[Gy] | Dmin [Gy] | Dmoy [Gy] |
| PTV70 | 200.900 | 74.986 | 52.855 | 69.562 |
| Chiasma | 1.400 | 2.441 | 2.358 | 2.111 |
| Nerfs optique droit | 0.900 | 2.345 | 1.179 | 2.020 |
| Nerfs optique gauche | 1.000 | 2.468 | 2.156 | 2.170 |
| Moelle épinière | 37.900 | 46.882 | 0.564 | 24.938 |
| Tronc cérébrale | 24.800 | 54.659 | 6.714 | 44.310 |
| L’Œil droite | 8.100 | 46.598 | 2.107 | 11.372 |
| L’Œil gauche | 7.900 | 39.462 | 2.020 | 9.697 |
| Cristallin droit | 0.100 | 9.032 | 5.550 | 7.220 |
| Cristallin gauche | 0.100 | 7.914 | 5.281 | 6.426 |
Tab 3.12 : Les différents résultats de la Dmoy ,Dmax ,Dmin et les volumes.
L’indice d’homogénéité
𝐻(𝑅𝐶3𝐷) = 𝐷𝑚𝑎𝑥 − 𝐷𝑚𝑖𝑛 = 74.986 − 52.855 = 0.318
𝐷𝑚𝑜𝑦
69.562
L’indice de conformité
𝑉𝑃𝑇𝑉
𝑉𝑃𝑇𝑉
603.700
200.900
= 3.004
| Organe | gEUD[Gy] | NTCPgEUD | NTCPLyman | TCPgEUD |
| Tumeur | 72.064 | – | – | 50.179% |
| Moelle épinière | 31.241 | 0.000% | 0.823% | – |
| Tronc cérébrale | 48.7184 | 3.047% | 1.988% | – |
Tab 3.13 : Différente résultats de gEUD , NTCPLyman ,NTCPgEUD.
Comparaison des HDVs pour les 2 techniques
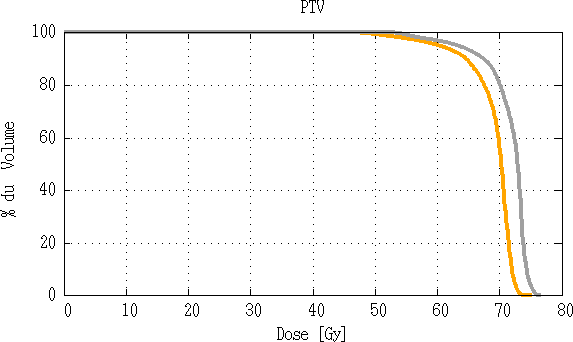
Fig 3.15 : Comparaison d’histogramme dose volume du PTV70.
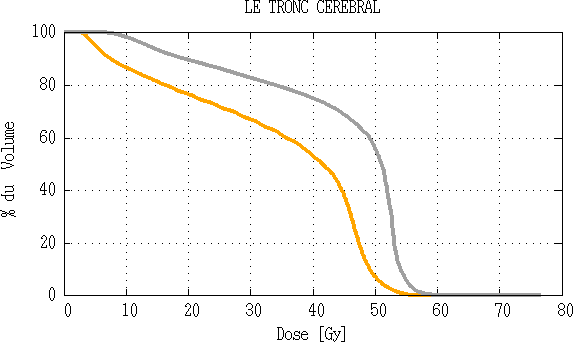
Fig 3.16 : Comparaison d’histogramme dose volume du tronc cérébral.
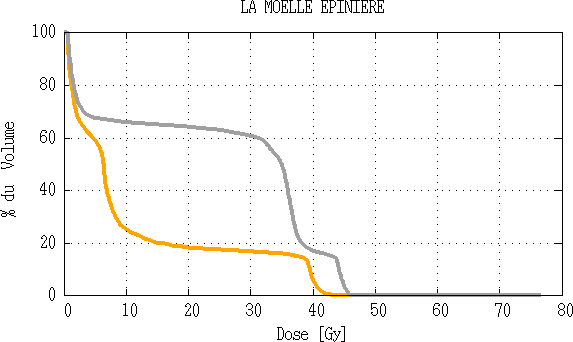
Fig 3.17 : Comparaison d’histogramme dose volume de la moelle épinière.
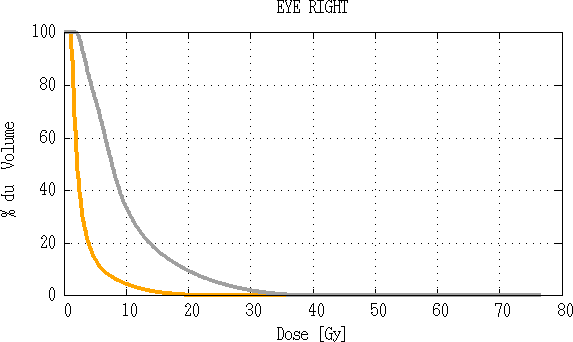
Fig 3.18 : Comparaison d’histogramme dose volume de l’œil droite.
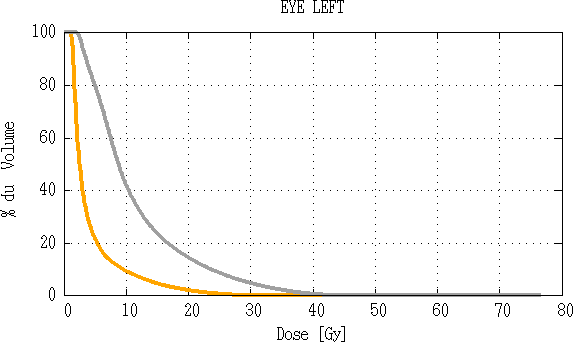
Fig 3.19 : Comparaison d’histogramme dose volume de l’œil gauche.
3th Patient
Analyse de la couverture des PTV à partir des dosimétries prévisionnelles
Sur les courbes isodoses en dosimétrie RC3D, on trouve que l’isodose 95% (66.5 Gy) couvre 87.1% du PTV70 pour la technique classique et 94.3% pour la technique 5 champs.
Analyses des OAR et PTV à partir des HDV et calcule des indices
Technique classique
La dose minimale reçue par le PTV70 est de 51.263 Gy, et la dose maximale est de 71.872 Gy. Les contraintes au niveau de la moelle, l’Œil, les nerfs optiques et le tronc cérébrale sont respectées.
A partir des données mesurées en C.R.O, les volumes, les doses moyennes minimales, maximales délivrées aux organes à risque et au PTV sont résumées dans le tableau suivant :
| Organe | Volume [cm3] | Dmax[Gy] | Dmin [Gy] | Dmoy [Gy] |
| PTV70 | 75.900 | 71.872 | 51.263 | 68.933 |
| Chiasma | 3.200 | 38.745 | 7.021 | 20.116 |
| Nerfs optique droit | 1.200 | 2.541 | 1.791 | 2.019 |
| Nerfs optique gauche | 1.200 | 2.355 | 1.701 | 2.001 |
| Moelle épinière | 47.900 | 45.547 | 0.219 | 14.334 |
| Tronc cérébrale | 31.700 | 55.783 | 1.879 | 23.940 |
| L’Œil droite | 10.100 | 38.355 | 0.889 | 6.460 |
| L’Œil gauche | 10.300 | 31.285 | 0.853 | 4.983 |
| Cristallin droit | 0.300 | 2.724 | 1.190 | 1.761 |
| Cristallin gauche | 0.300 | 2.362 | 1.021 | 1.519 |
Tab 3.14 : Les différents résultats de la Dmoy ,Dmax ,Dmin et les volumes.
L’indice d’homogénéité
𝐻(𝑅𝐶3𝐷) = 𝐷𝑚𝑎𝑥 − 𝐷𝑚𝑖𝑛 = 71.872 − 51.263 = 0.298
𝐷𝑚𝑜𝑦
68.933
L’indice de conformité
𝑉𝑃𝑇𝑉
𝑉𝑃𝑇𝑉
473.400
101.100
= 4.682
| Organe | gEUD[Gy] | NTCPgEUD | NTCPLyman | TCPgEUD |
| Tumeur | 69.004 | – | – | 46.452% |
| Moelle épinière | 30.541 | 0.000% | 0.869% | – |
| Tronc cérébrale | 27.761 | 0.099% | 0.736% | – |
Tab 3.15 : Différente résultats de gEUD , NTCPLyman ,NTCPgEUD.
Technique 5 champs
La dose minimale reçue par le PTV70 est de 58.672 Gy et la dose maximale est de 73.876 Gy. Les contraintes au niveau de la moelle, l’Œil, les nerfs optiques et le tronc cérébrale sont respectées.
A partir des données mesurées en C.R.O, les volumes, les doses moyennes minimales, maximales délivrées aux organes à risque et au PTV sont résumées dans le tableau suivant :
| Organe | Volume [cm3] | Dmax[Gy] | Dmin [Gy] | Dmoy [Gy] |
| PTV70 | 75.900 | 73.876 | 58.672 | 71.215 |
| Chiasma | 3.200 | 36.025 | 6.206 | 17.943 |
| Nerfs optique droit | 1.200 | 2.541 | 1.791 | 2.019 |
| Nerfs optique gauche | 1.200 | 2.355 | 1.701 | 2.001 |
| Moelle épinière | 47.900 | 46.669 | 0.219 | 15.129 |
| Tronc cérébrale | 31.700 | 58.070 | 2.585 | 31.484 |
| L’Œil droite | 10.100 | 38.433 | 1.321 | 7.640 |
| L’Œil gauche | 10.300 | 32.839 | 1.216 | 5.806 |
| Cristallin droit | 0.300 | 4.674 | 1.736 | 2.796 |
| Cristallin gauche | 0.300 | 3.262 | 1.493 | 2.162 |
Tab 3.16 : Les différents résultats de la Dmoy ,Dmax ,Dmin et les volumes.
L’indice d’homogénéité
𝐻(𝑅𝐶3𝐷) = 𝐷𝑚𝑎𝑥 − 𝐷𝑚𝑖𝑛 = 73.876 − 58.672 = 0.213
𝐷𝑚𝑜𝑦
71.215
L’indice de conformité
𝑉𝑃𝑇𝑉
𝑉𝑃𝑇𝑉
475.300
101.100
= 4.712
| Organe | gEUD[Gy] | NTCPgEUD | NTCPLyman | TCPgEUD |
| Tumeur | 69.944 | – | – | 48.369% |
| Moelle épinière | 28.541 | 0.000% | 0.701% | – |
| Tronc cérébrale | 29.761 | 0.095% | 0.939% | – |
Tab 3.17 : Différente résultats de gEUD , NTCPLyman , NTCPgEUD.
Résultats en moyenne
Analyse de la couverture des PTV à partir des dosimétries prévisionnelles
Sur les courbes isodoses de l’ensemble des résultats, l’isodose 95% (66.5 Gy) couvre 87.5% ± 3.7% du PTV70 pour la technique classique et 94.7%±1.8% pour la technique 5 champs.
Technique classique
La dose minimale reçue par le PTV70 dans l’ensemble des résultats est de 50.251±3.891 Gy et la dose maximale est de 73.718±1.646 Gy. Les contraintes au niveau de la moelle, l’Œil, les nerfs optiques et le tronc cérébrale sont respectées pour tous les patients.
A partir des données mesurées en C.R.O, les volumes, les doses moyennes minimales, maximales délivrées aux organes à risque et au PTV sont résumées dans le tableau suivant :
| Organe | Volume [cm3] | Dmax[Gy] | Dmin [Gy] | Dmoy [Gy] |
| PTV70 | 125.333±66.471 | 74.385±2.260 | 50.25±13.891 | 69.785±1.072 |
| Chiasma | 2.133±0.945 | 14.619±2.894 | 4.007± 2.625 | 20.116 ±1.171 |
| Nerfs optique droit | 0.866±0.351 | 2.508±0.191 | 1.7480±0.129 | 2.018±0.013 |
| Nerfs optique gauche | 1.100±0.100 | 2.270±0.136 | 1.618±0.198 | 2.001±0.195 |
| Moelle épinière | 40.533±6.465 | 43.065±1.127 | 1.081±1.091 | 14.533±3.695 |
| Tronc cérébrale | 30.366±1.738 | 50.203±4.142 | 2.084±0.604 | 26.660±6.832 |
| L’Œil droite | 10.000±1.852 | 24.093±19.467 | 0.837±0.229 | 3.953±2.648 |
| L’Œil gauche | 9.566±1.446 | 21.614±17.381 | 0.789±0.217 | 3.036±2.009 |
| Cristallin droit | 0.200±0.100 | 1.864±0.909 | 1.067±0.314 | 1.402±0.510 |
| Cristallin gauche | 0.200±0.100 | 1.728±0.797 | 0.959±0.304 | 1.278±0.467 |
Tab 3.18 : Les différents résultats de la Dmoy ,Dmax ,Dmin et les volumes pour tous les patients.
L’indice d’homogénéité :
𝐻(𝑅𝐶3𝐷) = 0.343 ± 0.069
L’indice de conformité :
𝐶𝐼 = 3.266 ± 1.018
| Organe | gEUD[Gy] | NTCPgEUD[%] | NTCPLyman[%] | TCPgEUD[%] |
| Tumeur | 69.110±0.158 | – | – | 44.839±2.745 |
| Moelle épinière | 32.428±2.685 | 0.001±0.000 | 0.893±0.084 | – |
| Tronc cérébrale | 35.667±7.173 | 0.241±0.216 | 0.593±0.337 | – |
Tab 3.19 : Différente résultats de gEUD , NTCPLyman ,NTCPgEUD pour tous les patients.
Technique 5 champs
La dose minimale reçue par le PTV70 dans l’ensemble des résultats est de 55.929±2.922 Gy et la dose maximale est de 75.418±1.343 Gy. Les contraintes au niveau de la moelle, l’Œil, les nerfs optiques et le tronc cérébrale sont respectées pour tous les patients.
A partir des données mesurées en C.R.O, les volumes, les doses moyennes minimales, maximales délivrées aux organes à risque et au PTV sont résumées dans le tableau suivant :
| Organe | Volume [cm3] | Dmax[Gy] | Dmin [Gy] | Dmoy [Gy] |
| PTV70 | 125.333±66.471 | 74.587±0.617 | 55.929±2.922 | 70.446±0.832 |
| Chiasma | 2.133±0.945 | 13.725±1.312 | 2.274±0.021 | 7.517±9.031 |
| Nerfs optique droit | 0.866±0.351 | 2.496±0.134 | 1.604±0.369 | 2.044±0.042 |
| Nerfs optique gauche | 1.100±0.100 | 2.412±0.056 | 1.827±0.286 | 2.056±0.098 |
| Moelle épinière | 40.533±6.465 | 45.937±1.455 | 0.850±0.813 | 14.018±12.754 |
| Tronc cérébrale | 30.366±1.738 | 52.920±2.562 | 3.744±2.592 | 35.759±7.405 |
| L’Œil droite | 10.000±1.852 | 29.108±23.578 | 1.403±0.665 | 6.797±5.048 |
| L’Œil gauche | 9.566±1.446 | 24.743±20.033 | 1.346±0.618 | 5.591±4.217 |
| Cristallin droit | 0.200±0.100 | 4.957±3.940 | 2.505±2.367 | 3.693±3.174 |
| Cristallin gauche | 0.200±0.100 | 4.092±3.481 | 2.737±2.678 | 3.195±2.857 |
L’indice d’homogénéité :
𝐻(𝑅𝐶3𝐷) = 0.261 ± 0.052
L’indice de conformité :
𝐶𝐼 = 3.673 ± 0.912
| Organe | gEUD[Gy] | NTCPgEUD[%] | NTCPLyman[%] | TCPgEUD[%] |
| Tumeur | 70.910±1.072 | – | – | 48.325±1.876 |
| Moelle épinière | 29.441±1.558 | 0.000±0.000 | 0.835±0.141 | – |
| Tronc cérébrale | 39.703±9.512 | 1.165±0.634 | 1.094±0.827 | – |
Tab 3.21 : Différente résultats de gEUD , NTCPLyman ,NTCPgEUD.
Discussion
Nous voyons donc que la technique 5 champs offre les meilleurs résultats pour le PTV, l’isodose 95% de la technique 5 champs couvre 96% du PTV pour le 1er patient et 93.1 % du PTV pour le 2eme patient, par rapport à la technique classique, l’isodose 95% couvre 91.4% du PTV pour le 1er patient et 84.1% pour le 2eme patient.
Les résultats montrent que la dose maximale est faible avec la technique 5 champs, elle ne dépasse pas 105-107% de dose (74.042 Gy-74.986Gy). Par contre avec la technique classique le point chaud est de 76.251 Gy (109%), ce qui est intolérable dans le traitement du cancer Nasopharynx. Et ils montrent également en ce qui concerne les organes à risque les tolérances de dose sont respectées, effectivement la dose maximale de la moelle ne dépasse pas les 50 Gy, également la dose de tolérance au niveau du tronc est respectée < 64Gy pour les deux techniques.
L’avantage majeure de la technique classique est qu’elle permet des doses faibles au niveau du tronc cérébrale et des globes oculaires œil et cristallin, ce qui n’est pas le cas avec la technique 5 champs.
Or cette dernière permet d’avoir une meilleure homogénéité de dose vu l’équivalent de dose uniforme (gEUD) ainsi l’indice d’homogénéité est inférieur à ce de la technique classique, mais la conformation de la dose au volume tumoral dans cette dernière est plus conformationnelle par rapport à la technique 5 champs.
Les probabilités de complication des tissus sains sont pratiquement identiques pour les deux techniques. Pourtant la probabilité de control tumoral de technique 5 champs, est par rapport à la technique classique.
L’utilisation des faisceaux d’électrons dans la technique classique oblige l’utilisation d’applicateur ce qui rend le temps de traitement assez large par rapport à la technique 5 champs, il peut prendre environ 20 min / patient contre 10 min/patient.
| Comparaison | |
| Technique classique | Bonne couverture du PTV. Faible homogénéité. Faible toxicité aux OARs. Bonne conformation. Durée des séances longues. |
| Technique 5 champs | Très bonne couverture du PTV. Bonne homogénéité. Moyenne toxicité aux OARs Faible conformation. Durée des séances courtes. |
Tab 3.22 : Récapitulatif des propriétés de chaque technique.
Conclusion générale
L’utilisation des rayonnements ionisants en radiothérapie externe nécessite la plus grande vigilance de la part du radiophysicien médical lors de chaque traitement or le pronostic vital du patient est mis à contribution.
L’importance de la radiothérapie dans le traitement des cancers, met en œuvre des appareillages et des techniques complexes. La précision des doses à délivrer pour éviter les complications et les récidives impose un choix et un contrôle très strict des équipements et des techniques. L’outil de planification de traitement TPS est directement en rapport avec la dose délivrée aux patients. Il est donc primordial que les calculs du TPS concordent avec le faisceau d’irradiation brut de l’accélérateur linéaire.
Au cours de notre étude, deux voies sont utilisées dans la prise en charge du cancer du Nasopharynx :
- • La technique classique.
- • La technique 5 champs.
Notre objectif est de faire une comparaison entre ces deux techniques et de conclure qui semble la plus efficace. Nous avons pu observer que la technique 5 champs présente de bons résultats dosimétriques que la technique classique et de mauvais résultats au niveau de la toxicité et la conformation du volume cible.
Éventuellement les inconvénients d’une technique présentent les avantages de l’autre, bien que la technique classique présente des avantages non négligeables. A ne pas oublier le facteur temps et l’utilisation d’applicateur d’électrons dans la technique classique augmente le risque de commettre des erreurs par le manipulateur.
Grosso modo, les résultats obtenus dans cette évaluation dosimétrique confirment que la technique 5 champs présente des avantages par rapport à la technique classique dans la couverture du volume cible, l’homogénéité et le contrôle tumoral mais elle présente aussi des inconvénients pour la conformation de la dose et la toxicité des organes à risques, qui sont les avantages de la technique classique. En outre, on ne peut pas conclure qu’une technique est plus efficace que l’autre, puisque chacune présente ses propres avantages et inconvénients.
9 Pour la région ORL, c’est tellement difficile d’avoir une dose dans PTV en 95% et 107% sans surdoser les OARs, on a essayé de trouver un compromis entre la couverture du PTV et la préservation des OARs.
Les cancers du Nasopharynx demeurent un sérieux problème de santé publique dans nombreux pays. Les rechutes métastatiques et locorégionales constituaient la cause principale de décès. La radiothérapie constitue la base de traitement de ce cancer. L’adjonction de la chimiothérapie néo adjuvante ou concomitante a permis d’améliorer les résultats thérapeutiques sur le plan de contrôle local et survie globale. Cependant, des études sont nécessaires pour standardiser le traitement des cancers du Nasopharynx.